| Ok(n)o wiedzy genetycznej - nauka, nadzieje, kontrowersje, aktualności, ciekawostki, kontakty |
 |
 |
| Nowiny z dziedziny nauki - nadzieje, oczekiwania |
Retinitis Pigmentosa
| Zespół Ushera
| AMD
| Stargardt
| Goście RF
Artykuły, publikacje | Ciekawostki | Geny z humorem | Linki | Listy do RETINY | Słowniczek
Strona główna
Spis treści
Terapia genowa - nowa strategia walki z dziedziczną ślepotą
Nowość w okulistyce – soczewka Eyemax mono do plamki żółtej
Pierwsza transplantacja siatkówki z komórek macierzystych iPS od dawcy
Optygenetyka - DNA glonów przywróci niewidomym wzrok?
Retinopatia barwnikowa - przełomowe dokonanie genetyków
Wielki krok do przodu w walce z AMD z wykorzystaniem iPS
Dieta i ćwiczenia fizyczne przyczyniają się do zdrowia oczu
Wstrzyknięcie genu nadzieją w leczeniu Parkinsona
Alarm dla technologii biomedycznych związany z zastosowaniem grafenu
Terapia genowa u osób z wrodzoną ślepotą Lebera (LCA)
Japończycy w niezwykłej walce z AMD i rakiem, orężem - iPS
Projekt „Grafen” ważny dla technologii implantów siatkówki?
Nagroda Nobla w dziedzinie medycyny
Chemiczny włącznik wzroku? Niezwykła wiadomość naukowa!
FDA ostrzega przed niebezpieczeństwem groźnej infekcji oka po injekcji Avastinu z porcjowanych fiolek
Komórki macierzyste skóry odbudowują soczewkę oka
Uwagi dot. stosowania kwasu walproinowego w barwnikowym zwyrodnieniu siatkówki
Sztuczne oko coraz bliżej
Enzym DICER1 kluczem do skutecznej walki z AMD?
W USA zmniejsza się zachorowalność na AMD
Nowa strategia walki z alzheimerem
Skuteczna terapia w chorobie Stargardta - bliżej niż dalej
Przeszczep biosyntetycznej rogówki przywraca wzrok
Resweratrol w walce z otyłością, przeciw retinopatii cukrzycowej i AMD
Luteina spowalnia proces ograniczenia pola widzenia w retinitis pigmentosa?
Nowy ultracienki chip - możliwość zastosowania w implantach siatkówki oka
Wpływ Aspiryny na AMD - nie pomaga, nie szkodzi
Wyniki porównawczych badań preparatów: Bevacizumab (Avastin) i Ranibizumab (Lucentis)
NT-501 - nadzieja dla chorych na Retinitis Pigmentosa
Nowa metoda badania oka
Substancja regenerująca siatkówkę
Komórki macierzyste w leczeniu chorób oczu
Nadzieja w zastrzyku, który przywróci wzrok
Białko Robo4 szansą w walce o wzrok
Argus II - szansa na przywrócenie wzroku
Przepis na widzenie?
ARCHIWUM ARTYKUŁÓW: „Nowiny z dziedziny nauki”
Artykuły, publikacje | Ciekawostki | Geny z humorem | Linki | Listy do RETINY | Słowniczek
Strona główna
Spis treści
Terapia genowa - nowa strategia walki z dziedziczną ślepotą
Nowość w okulistyce – soczewka Eyemax mono do plamki żółtej
Pierwsza transplantacja siatkówki z komórek macierzystych iPS od dawcy
Optygenetyka - DNA glonów przywróci niewidomym wzrok?
Retinopatia barwnikowa - przełomowe dokonanie genetyków
Wielki krok do przodu w walce z AMD z wykorzystaniem iPS
Dieta i ćwiczenia fizyczne przyczyniają się do zdrowia oczu
Wstrzyknięcie genu nadzieją w leczeniu Parkinsona
Alarm dla technologii biomedycznych związany z zastosowaniem grafenu
Terapia genowa u osób z wrodzoną ślepotą Lebera (LCA)
Japończycy w niezwykłej walce z AMD i rakiem, orężem - iPS
Projekt „Grafen” ważny dla technologii implantów siatkówki?
Nagroda Nobla w dziedzinie medycyny
Chemiczny włącznik wzroku? Niezwykła wiadomość naukowa!
FDA ostrzega przed niebezpieczeństwem groźnej infekcji oka po injekcji Avastinu z porcjowanych fiolek
Komórki macierzyste skóry odbudowują soczewkę oka
Uwagi dot. stosowania kwasu walproinowego w barwnikowym zwyrodnieniu siatkówki
Sztuczne oko coraz bliżej
Enzym DICER1 kluczem do skutecznej walki z AMD?
W USA zmniejsza się zachorowalność na AMD
Nowa strategia walki z alzheimerem
Skuteczna terapia w chorobie Stargardta - bliżej niż dalej
Przeszczep biosyntetycznej rogówki przywraca wzrok
Resweratrol w walce z otyłością, przeciw retinopatii cukrzycowej i AMD
Luteina spowalnia proces ograniczenia pola widzenia w retinitis pigmentosa?
Nowy ultracienki chip - możliwość zastosowania w implantach siatkówki oka
Wpływ Aspiryny na AMD - nie pomaga, nie szkodzi
Wyniki porównawczych badań preparatów: Bevacizumab (Avastin) i Ranibizumab (Lucentis)
NT-501 - nadzieja dla chorych na Retinitis Pigmentosa
Nowa metoda badania oka
Substancja regenerująca siatkówkę
Komórki macierzyste w leczeniu chorób oczu
Nadzieja w zastrzyku, który przywróci wzrok
Białko Robo4 szansą w walce o wzrok
Argus II - szansa na przywrócenie wzroku
Przepis na widzenie?
ARCHIWUM ARTYKUŁÓW: „Nowiny z dziedziny nauki”
Nadzieja dla pacjentów z retinitis pigmentosa i... nie tylko dla nich! data publikacji - 9 września 2020 r.  Retinitis pigmentosa (RP) zwyrodnienie barwnikowe siatkówki jest najczęstszą formą dziedzicznej ślepoty. Monachijscy naukowcy skompensowali teraz niepowodzenie wadliwych genów u myszy podejściem do terapii genowej, aktywując w szczególności wycofane geny o podobnej funkcji. Retinitis pigmentosa (RP) zwyrodnienie barwnikowe siatkówki jest najczęstszą formą dziedzicznej ślepoty. Monachijscy naukowcy skompensowali teraz niepowodzenie wadliwych genów u myszy podejściem do terapii genowej, aktywując w szczególności wycofane geny o podobnej funkcji.W Niemczech dziedziczna choroba oczu pigmentosa, która jest spowodowana mutacjami w wielu różnych genach, dotyka do 40 000 osób. W zależności od wady genetycznej, ślepota nocna i pełzająca utrata pola widzenia występują aż do całkowitej ślepoty. Pierwsze metody terapeutyczne genów zostały niedawno zatwierdzone dla niektórych postaci choroby. Konwencjonalne terapie genowe mają jednak wady, które ograniczają ich potencjał. Dlatego zespół kierowany przez prywatnego wykładowcę Elvira Becirovica z Katedry Farmakologii Nauk Przyrodniczych w Monachium opracował nową strategię, w której wykorzystuje technologię CRISPR/Cas9 do reaktywacji wycofanych genów, które pełnią funkcje podobne do tych wadliwych genów. Prof. Dr Stylianos Michalakis z Kliniki Okulisty LMU w Monachium był również zaangażowany w rozwój. Pomyślnie przetestowali swoje nowe podejście do terapii genowej w modelu myszy, jak donoszą naukowcy w czasopiśmie Science Advances. Poprzednie strategie terapii genowej Obecnie w opracowywaniu terapii genowych stosuje się dwie strategie: W ramach suplementacji genów podejmowana jest próba zastąpienia wadliwego genu wersją nienaruszoną. Jednak obecnie jest to możliwe tylko w przypadku stosunkowo małych genów. Druga strategia ma na celu skorygowanie mutacji chorobotwórczych, ale zwykle musi ona być dostosowana do każdej indywidualnej mutacji. Ze względu na wysoki wysiłek i związane z tym koszty rozwoju, nie jest zatem możliwe szerokie wykorzystanie tej strategii. "Aby przezwyciężyć te ograniczenia, opracowaliśmy zupełnie nową strategię", mówi Becirovic. Wiele genów w ludzkim genomie ma podobne funkcje, ale często są aktywne w różnym czasie lub w różnych komórkach. "Naszym pomysłem było zrekompensowanie funkcji zmutowanego genu za pomocą tak zwanego systemu Cas9-VPR w celu ponownego zaangażowania wycofanych genów o podobnej funkcji w dotkniętych komórkach", mówi Becirovic. System Cas-9-VPR jest wariantem znanej technologii CRISPR/Cas9, za pomocą której genom można modyfikować bez jego cięcia. Test na modelu myszy z RP W mysim modelu z retinitis pigmentosa naukowcy z powodzeniem wykorzystali tę nową metodę: myszy posiadają mutację genu dla retopsyny pigmentu wzrokowego. Pigment ten jest produkowany wyłącznie w prętach, czyli w komórkach wizualnych, które są odpowiedzialne za widzenie w nocy i zmierzchu. Wstrzykując Cas9-VPR do pałeczek myszy, naukowcy włączyli geny ściśle związane z genem rodopsyny, które są zwykle aktywne w stożkach odpowiedzialnych za kolor i widzenie w ciągu dnia. "Pozwoliło nam to zrekompensować brak funkcji rodopsyny, spowolnić zwyrodnienie retinitis pigmentosa i poprawić funkcjonowanie siatkówki bez żadnych wykrywalnych skutków ubocznych", mówi Becirovic. Podejście również przydatne dla innych genów? Według naukowców nowe podejście można również zastosować do wielu innych genów i chorób dziedzicznych i oferuje zdecydowane korzyści w porównaniu z istniejącymi strategiami. "Biorąc pod uwagę szybko rosnące znaczenie terapii genowej i korzyści, jakie przynosi ona osobom dotkniętym chorobą, jesteśmy przekonani, że nasze podejście może wkrótce zostać zastosowane w kontekście wstępnych badań wykonalności klinicznej", mówi Becirovic. Oryginalna publikacja: Terapia genowa dziedzicznej ślepoty za pomocą aktywacji transkrypcyjnej za pośrednictwem dCas9-VPR. Sybille Böhm, Victoria Splith, Lisa Maria Riedmayr, René Dominik Rötzer, Gilles Gasparoni, Karl J. V. Nordström, Johanna Elisabeth Wagner, Klara Sonnie Hinrichsmeyer, Jörn Walter, Christian Wahl-Schott, Stefanie Fenske, Martin Biel, Stylianos Michalakis i Elvir Becirovic. Postępy naukowe 2020. źródło: PRO RETINA Deutschland e. V. |
Najnowocześniejsza soczewka wewnątrzgałkowa Eyemax Mono. Nowość w okulistyce! data publikacji - 18 maja 2019 r.  Do tej pory większość pacjentów z suchą formą zwyrodnienia plamki żółtej słyszała, że „nic się nie da zrobić”, żeby widzieli lepiej. Pomimo że nadal nie ma stuprocentowo skutecznego lekarstwa na suchą postać zwyrodnienia plamki żółtej, to jednak pacjentom, którzy na nią cierpią, wszczepienie Eyemax Mono może znacząco poprawić, a nawet przywrócić wzrok.
Do tej pory większość pacjentów z suchą formą zwyrodnienia plamki żółtej słyszała, że „nic się nie da zrobić”, żeby widzieli lepiej. Pomimo że nadal nie ma stuprocentowo skutecznego lekarstwa na suchą postać zwyrodnienia plamki żółtej, to jednak pacjentom, którzy na nią cierpią, wszczepienie Eyemax Mono może znacząco poprawić, a nawet przywrócić wzrok.Technologia innowacyjnej soczewki Eyemax Mono została opracowana przez dr Bobby’ego Quershi, który kieruje zespołem chirurgów okulistów oraz naukowców z London Eye Hospital Pharma. Jest to zespół lekarzy z ogromnym doświadczeniem w leczeniu pacjentów ze zwyrodnieniem plamki żółtej. W Polsce, jako pierwszy i na razie jedyny, soczewkę Eyemax Mono stosuje Szpital Okulistyczny Retina. Dla jakich pacjentów jest wskazana soczewka Eyemax Mono? Soczewka Eyemax Mono może pomóc pacjentom w suchych i niektórych mokrych formach zwyrodnienia plamki żółtej, oraz pacjentom z innymi formami chorób plamki, takimi jak: – cukrzycowe zwyrodnienie plamki, – otwór w plamce, – zwyrodnienie krótkowzroczne, – dziedziczne zwyrodnienia siatkówki, takie jak dystrofia Stargardta i Besta. Procedura wczepienia soczewki Eyemax Mono jest odpowiednia zarówno dla pacjentów, którzy wcześniej przeszli zabieg usunięcia zaćmy, jak i dla tych, którzy nie przechodzili takiej operacji. Jak działa soczewka Eyemax Mono? Soczewka działa jak mały teleskop. Dzięki niej obraz docierający do oka powiększa się, a następnie zostaje przeniesiony na zdrowsze części siatkówki wokół plamki. Daje to możliwość znacznej poprawy widzenia środkowego. Dzięki temu, że soczewka zapewnia wysoką jakość obrazu we wszystkich częściach plamki, mózg może pomagać oku wybrać obraz z najzdrowszej części siatkówki. Nawet jeśli choroba nadal postępuje, soczewka Eyemax Mono pracuje nadal. Powoduje, że mózg automatycznie odbiera najlepszą jakość obrazu dostępną na siatkówce. Daje nam to pewność, że soczewka utrzyma najlepsze widzenie, jakie plamka żółta oka może osiągnąć. Jak soczewka Eyemax Mono wpływa na polepszenie widzenia? Dzięki wszczepieniu tej soczewki pacjent może rozpoznawać rysy twarzy, czytać, a nawet prowadzić samochód. Procent poprawy widzenia, u niektórych osób większy, u innych mniejszy, zależy od rodzaju i zaawansowania schorzenia danego pacjenta. Jakie jest ryzyko? Ryzyko wszczepienia soczewki Eyemax Mono nie jest większe niż ryzyko operacji usunięcia zaćmy, czyli bardzo niewielkie. Jak wygląda procedura wszczepienia soczewki Eyemax Mono? Soczewka Eyemax Mono wielkością ani kształtem nie różni się od innych soczewek stosowanych przy operacjach zaćmy. Wszczepiamy ją do oka podczas zabiegu chirurgicznego (trwa on do 15 minut) bez konieczności pozostania na noc w szpitalu. W pierwszej dobie po zabiegu pacjent odbywa wizytę kontrolną. Powrót do zdrowia po zabiegu jest szybki i nie wymaga przestrzegania szczególnych zaleceń lekarskich. Przez około miesiąca po zabiegu pacjent stosuje krople, zazwyczaj takie same jak w przypadku operacji zaćmy. Zaleca się wszczepienie soczewki Eyemax Mono do obu oczu w krótkim odstępie czasu. Inaczej pacjent będzie widział obrazy różnej wielkości w każdym oku. Po operacji pacjenci mogą potrzebować nieco czasu, aby oswoić się z efektem lepszego widzenia. Pacjenci z mokrą postacią zwyrodnienia plamki żółtej, którzy tracą wzrok nagle w wyniku krwawienia pod siatkówką, potrzebują około 4 miesięcy na przyzwyczajenie się do efektów działania soczewki. Zalecane jest też, by pacjenci po operacji wszczepienia soczewki Eyemax Mono odczekali około 4 tygodni, zanim wyrobią sobie nowe okulary. Dlaczego warto wszczepić soczewkę Eyemax Mono? Czym soczewka Eyemax Mono różni się od innych soczewek wewnątrzgałkowych? Przede wszystkim: – poprawia zarówno widzenie na odległość, jak i zdolność czytania – u większości pacjentów widzenie do dali polepsza się średnio o ponad 3 linie, a widzenie bliskie o więcej niż 2 linie na tablicy testowej, u niektórych ta poprawa wynosi nawet 5 linii, – po wszczepieniu soczewki Eyemax Mono pacjenci są w stanie czytać o około 25% szybciej niż przed operacją, – mimo że soczewka nie przywraca w pełni wzroku oraz nie powstrzymuje rozwoju choroby, to jednak minimalizuje skutki nasilających się uszkodzeń siatkówki i utrzymuje najlepszy wzrok, jaki plamka żółta twojego oka może osiągnąć, – po wszczepieniu soczewki pacjenci czują się pewniejsi swojego widzenia. Ogólnie mówiąc: następuje poprawa jakości obrazu w zdrowszych częściach siatkówki. Soczewka Eyemax Mono a okulary Efekt powiększenia obrazu dzięki soczewce Eyemax Mono może być spotęgowany dzięki używaniu okularów o umiarkowanej mocy. Pacjenci po wszczepieniu soczewki Eyemax Mono potrzebują na ogół dwóch par okularów: do pracy z bliska, i drugich, do dali. źródło: Retina.pl - Przychodnia i Szpital Okulistyczny Retina (kontakt tel. 693 722 448 lub 22 664 44 33) |
Pierwsza transplantacja siatkówki z komórek macierzystych iPS od dawcy data publikacji - 10 maja 2017 r.
Operacja odbyła się w Kobe City Medical Center General Hospital 28 marca 2017 roku. Przeprowadził ją Yasuo Kurimoto, ordynator tamtejszego oddziału okulistyki. Zespołowi przewodniczyła Masayo Takahashi z instytutu badań Riken. Do operacji wykorzystano zapasy indukowanych pluripotencjalnych komórek macierzystych (iPS) zgromadzone przez Uniwersytet w Kioto. Powstały one na skutek laboratoryjnej modyfikacji wyspecjalizowanych komórek. Jak podaje portal EuroStemCell, z ich wykorzystaniem można utworzyć każdy rodzaj komórek. To pierwsza na świecie sytuacja, gdy do transplantacji siatkówki wykorzystane zostały komórki niepochodzące od pacjenta poddanemu zabiegowi. Transplantacja została przeprowadzona u pacjenta po 60. roku życia, wybranego spośród pięciu innych kandydatów również dotkniętych zwyrodnieniem plamki żółtej. Przeszczep miał zapobiec dalszemu rozwojowi choroby, która może prowadzić do całkowitej utraty wzroku. Trwająca godzinę operacja została przeprowadzona bez żadnych komplikacji, jednak przez najbliższe trzy lata pacjent pozostanie pod kontrolą lekarzy. Ma to pomóc uniknąć odrzucenia przeszczepionych komórek siatkówki. Dopiero po tym czasie będzie można powiedzieć, że operacja się powiodła. Komórki iPS wykorzystane do transplantacji zostały dobrane tak, aby zminimalizować ryzyko odrzucenia. W 2014 roku została wykonana operacja z użyciem komórek pacjenta, który podlegał przeszczepowi, a przygotowanie do zabiegu trwało 10 miesięcy. Wykorzystanie komórek macierzystych od dawcy redukuje czas przygotowań do miesiąca oraz pozwala obniżyć koszty operacji. Metoda ma zostać wykorzystana jeszcze przynajmniej u czterech pacjentów. Jeżeli procedura okaże się efektywna i bezpieczna, lekarze będą mogli decydować się na nią częściej. Według prestiżowego czasopisma naukowego „Nature” sukces metody może przyczynić się do utworzenia banków gotowych komórek macierzystych. Shinya Yamanaka, laureat Nagrody Nobla za odkrycie metody tworzenia komórek iPS, który obecnie jest w trakcie tworzenia banku tychże komórek, komentuje: Podczas gdy w Stanach Zjednoczonych podjęto wiele prób klinicznych z wykorzystaniem zarodkowych komórek macierzystych, zarówno Stany, jak i inne kraje uważnie obserwują wszystko, co związane z użyciem komórek iPS przez Japonię. źródło: japonia-online.pl/news/5473; opracowanie: Agnieszka Brzozowska Wielki krok do przodu w walce z AMD z wykorzystaniem iPS Japończycy w niezwykłej walce z AMD i rakiem, orężem - iPS Nagroda Nobla w dziedzinie medycyny |
data publikacji - 1 marca 2016 r.  Pierwszymi pacjentami poddanymi eksperymentalnej kuracji mają być ludzie, którzy utracili wzrok z powodu barwnikowego zwyrodnienia siatkówki (retinitis pigmentosa) - choroby uszkadzającej fotoreceptory w naszym oku - czopki i pręciki. Naukowcy tym razem nie będą próbowali odbudować tych komórek lecz raczej chcą doprowadzić do tego by znajdujące się głębiej w oku komórki zwojowe stały się światłoczułe i by przesyłały sygnały o świetle do mózgu, dzięki czemu mogły po prostu przejąć całkowicie rolę uszkodzonych pręcików i czopków. Pierwszymi pacjentami poddanymi eksperymentalnej kuracji mają być ludzie, którzy utracili wzrok z powodu barwnikowego zwyrodnienia siatkówki (retinitis pigmentosa) - choroby uszkadzającej fotoreceptory w naszym oku - czopki i pręciki. Naukowcy tym razem nie będą próbowali odbudować tych komórek lecz raczej chcą doprowadzić do tego by znajdujące się głębiej w oku komórki zwojowe stały się światłoczułe i by przesyłały sygnały o świetle do mózgu, dzięki czemu mogły po prostu przejąć całkowicie rolę uszkodzonych pręcików i czopków.Terapia opracowana na Wayne State University realizowana ma być przez firmę RetroSense, która z pomocą zmodyfikowanego genetycznie wirusa wprowadzić ma do oka pochodzące od glonów DNA odpowiadające za produkcję światłoczułych białek. W ten sposób powstać ma kilkaset tysięcy światłoczułych komórek, ale jest jeden minus - są one wrażliwe tylko na światło niebieskie, a zatem pacjenci odzyskają wizję czarno-białą. Technika ta została już sprawdzona wcześniej na myszach i okazała się ona skuteczna, lecz z wiadomych przyczyn nie wiemy do końca jak dobry wzrok posiadają zwierzęta, którym dało się go przywrócić. Tego będziemy mogli dowiedzieć się już niedługo, gdy eksperyment na ludziach się zakończy. Czekamy zatem z niecierpliwością na efekt końcowy tych badań. Możliwość wykorzystania światła do wybiórczego kontrolowania aktywności neuronów po raz pierwszy zasugerował Francis Crick w 1999. W 2002 roku po raz pierwszy opisano uzyskanie światłoczułych neuronów metodami inżynierii genetycznej. Optogenetyka ma mieć szerokie zastosowanie terapeutyczne, w tym m.in. choroby Parkinsona, uzależnień (np. alkoholizm) i innych schorzeń natury neurologicznej. źródła: MIT Technology Review, PRO Retina Deutschland e.V., Dolinabiotechnologiczna.pl |
data publikacji - 14 lutego 2016 r. Opracowana niedawno metoda precyzyjnej edycji genów pozwoliła naukowcom na naprawę genu wywołującego retinopatię barwnikową. Zmienione zostały komórki macierzyste chorego, więc teoretycznie można by je wszczepić do jego siatkówki bez obawy o odrzucenie.  Zespół badaczy z University of Iowa oraz Columbia University Medical Center wykorzystał opracowaną przed trzema laty technikę o nazwie CRISPR/Cas9. Uznawana jest ona za przełom w inżynierii genetycznej, gdyż pozwala na nieosiągalną dotąd precyzję w manipulowaniu DNA w komórkach. Zespół badaczy z University of Iowa oraz Columbia University Medical Center wykorzystał opracowaną przed trzema laty technikę o nazwie CRISPR/Cas9. Uznawana jest ona za przełom w inżynierii genetycznej, gdyż pozwala na nieosiągalną dotąd precyzję w manipulowaniu DNA w komórkach.W swoim eksperymencie uczeni pobrali komórki skóry pacjenta, po czym zmienili je w komórki macierzyste. Następnie skorygowali obecny w nich genetyczny błąd, jaki prowadzi do rozwoju retinopatii barwnikowej (przyp. red RF.: konkretnie chodzi o barwnikowe zwyrodnienie siatkówki - retinitis pigmentosa) sprzężonej z chromosomem X (XLRP). Udało im się zmodyfikować 13 proc. komórek, co jak twierdzą, pozwala na praktyczne wykorzystanie metody. Ważne jest, że komórki zostały pozyskane od chorej osoby. „Dzięki edycji genów ludzkich komórek metodą CRISPR, teoretycznie, po naprawie specyficznego błędu genetycznego możemy przeszczepić nowe, zdrowe komórki, które pochodzą od pacjenta.” - mówi prof. Vinit Mahajan z University of Iowa. „Choroby siatkówki są przy tym doskonałym modelem dla terapii z użyciem komórek macierzystych, ponieważ dysponujemy zaawansowanymi technikami chirurgicznymi, które pozwalają na wszczepienie komórek dokładnie tam, gdzie są potrzebne” - kontynuuje naukowiec. Zanim nowa metoda doprowadzi do terapii, potrzebne oczywiście będą dalsze testy. Konieczne jest np. sprawdzenie, czy rzeczywiście modyfikacji ulega wyłącznie wybrany gen. Badacze są jednak dobrej myśli. „Uważam, że jest nadzieja dla pacjentów z tą degeneracyjną chorobą siatkówki” - mówi inny z autorów eksperymentu, prof. Alexander Bassuk. źródła: Puls Medycyny (materiał opublikowany w RF dzięki uzgodnieniu z redakcją portalu Puls Medycyny, za co bardzo dziękuję - red. Piotr Stanisław Król). Więcej informacji na ten temat (j. ang.): http://www.nature.com/articles/srep19969 |
data publikacji - 21 października 2014 r. W ubiegłym roku, 16 marca 2013, opublikowany został na stronie RETINA FORUM artykuł pt. "Japończycy w niezwykłej walce z AMD i rakiem, orężem - iPS" (indukowane pluripotencjalne komórki macierzyste, ang.: iPSC - induced pluripotent stem cells). Jest to rewolucja w badaniach genetycznych, wielka nadzieja w medycynie. W 2006 roku Shinya Yamanaka zaprezentował w świecie nauki swoje niezwykłe odkrycie, które wykazało, że dojrzałe komórki organizmu można cofnąć w rozwoju do etapu komórek macierzystych, które w kolejnym etapie mogą być przekształcane w dowolne, wybrane komórki organizmu. W 2012 roku Yamanaka otrzymał za to wspaniałe osiągnięcie naukowe Nagrodę Nobla (link na końcu art.).  We wrześniu 2014 r. ukazały się w wielu mediach na świecie informacje pochodzące z raportu Instytutu RIKEN w Kobe, w Japonii, że w kraju kwitnącej wiśni rozpoczęto pierwsze badanie kliniczne z wykorzystaniem iPS na pacjencie z AMD, zaawansowanym zwyrodnieniem plamki żółtej związanej z wiekiem, tzw. odmianą "mokrą". Dokonano przeszczepu tkanki nabłonka barwnikowego siatkówki oka, która powstała z komórek iPS (wcześniej przeprowadzano je na zwierzętach doświadczalnych). We wrześniu 2014 r. ukazały się w wielu mediach na świecie informacje pochodzące z raportu Instytutu RIKEN w Kobe, w Japonii, że w kraju kwitnącej wiśni rozpoczęto pierwsze badanie kliniczne z wykorzystaniem iPS na pacjencie z AMD, zaawansowanym zwyrodnieniem plamki żółtej związanej z wiekiem, tzw. odmianą "mokrą". Dokonano przeszczepu tkanki nabłonka barwnikowego siatkówki oka, która powstała z komórek iPS (wcześniej przeprowadzano je na zwierzętach doświadczalnych).Zespół kierowany przez okulistę, Masayo Takahashi, przedstawił program badawczy w zeszłym roku i rozpoczął przygotowania do zabiegu. W skrócie - najpierw pobrane od pacjenta próbki skóry są izolowane z fibroblastów, a następnie przeznaczone do wygenerowania komórek iPS, które z kolei są "przetwarzane" w komórki nabłonka barwnikowego siatkówki oka. Jak informuje Instytut RIKEN, pierwsza tego typu operacja w świecie nauki przebiegła pomyślnie. Klaster komórek o wymiarach 1,3 × 3 mm został przeszczepiony do oka siedemdziesięcioletniego pacjenta z AMD. Nie było żadnego większego krwawienia lub powikłań. W ramach kontynuacji badań mają być przeprowadzane kolejne przeszczepy. Pacjenci poddawani będą badaniom kontrolnym co miesiąc zaraz po zabiegu w pierwszym półroczu, a następnie co dwa miesiące; w drugiej połowie roku: na ostrość widzenia, ciśnienie wewnątrzgałkowe, i za pomocą technik obrazowania, na wygląd punktu wszczepienia komórek. Pacjenci będą poddawani badaniom przez następnie trzy lata. Badania nie są pozbawione ryzyka wystąpienia nowotworów, ponieważ istnieje obawa, że komórki iPS mogą indukować powstawanie guzów. W badaniach przeprowadzonych na myszach nie wykazano guzów nowotworowych powstałych z komórek wytworzonych z iPS. Ryzyko jest niewielkie, ale nie można tego wykluczyć, badania naukowe muszą w stu procentach wykazać efekt końcowy, miejmy nadzieję, że jak najbardziej pozytywny. Od dwóch lat z uwagą śledzimy postępy w tej niezwykłej gałęzi badań genetycznych, która "...otwiera drogę do tworzenia części zamiennych człowieka, tych części, które nam się psują. Opracowaną [...] procedurę można wykorzystać absolutnie do wszystkiego. Można naprawiać zniszczone mięśnie serca, można tworzyć nowe organy, można tworzyć nową nerkę. To zresztą już robiono na modelach zwierzęcych" - powiedział prof. Piotr Stępień z Instytutu Biochemii i Biofizyki PAN oraz Instytutu Genetyki i Biotechnologii Uniwersytetu Warszawskiego. Obiecujemy naszym Czytelnikom, że każdą nową wiadomość w tym zakresie natychmiast opublikujemy na stronie RETINA FORUM. Piotr Stanisław Król źródła: raport Instytutu RIKEN w Kobe, Pro Retina Deutschland e.V. Wcześniejsze informacje w tym zakresie na stronie RETINA FORUM: "Japończycy w niezwykłej walce z AMD i rakiem, orężem - iPS" "Nagroda Nobla w dziedzinie medycyny 2012 r." |
przyczyniają się do zdrowia oczu data publikacji - 2 września 2014 r.  Komunikat prasowy Federalnego Związku Niemieckich Okulistów (BVA) z połowy 2014 roku potwierdza zalecenia od lat propagowane na stronie RETINA FORUM - codzienny energiczny spacer (uwaga - na stronie RF jest również informacja naukowców o pozytywnym działaniu joggingu, KLIKNIJ) lub jazda na rowerze, dużo witamin w diecie, a także czasami kieliszek czerwonego wina - mają bardzo pozytywny wpływ na ogólne zdrowie, w tym na, co jest niezwykle istotne, zachowanie jak najdłużej dobrego wzroku. Komunikat prasowy Federalnego Związku Niemieckich Okulistów (BVA) z połowy 2014 roku potwierdza zalecenia od lat propagowane na stronie RETINA FORUM - codzienny energiczny spacer (uwaga - na stronie RF jest również informacja naukowców o pozytywnym działaniu joggingu, KLIKNIJ) lub jazda na rowerze, dużo witamin w diecie, a także czasami kieliszek czerwonego wina - mają bardzo pozytywny wpływ na ogólne zdrowie, w tym na, co jest niezwykle istotne, zachowanie jak najdłużej dobrego wzroku.Korzystny trening wytrzymałościowy Dowody, że umiarkowane ćwiczenia są dobre dla siatkówki oka dostarczyli amerykańscy lekarze prowadzący badania na myszach, których siatkówki zostały uszkodzone przez ostre światło. Jedna grupa biegała godzinę dziennie w umiarkowanym tempie na laboratoryjnej, doświadczalnej bieżni; druga grupa myszy pozostawała bez treningu. U "aktywnych sportowo" zwierząt struktury i funkcje siatkówki oka zachowały lepszy stan. Badacze doszli do wniosku, że trening wytrzymałościowy chroni siatkówkę. "Regularne ćwiczenia mogą mieć wpływ na związane z wiekiem zmiany plamki żółtej oka, które są często odpowiedzialne za chorobę AMD" - stwierdził dr Daniel Pauleikhoff ze Związku Niemieckich Okulistów. Bogata w witaminy dieta chroni nasz wzrok Od lat wiadomo, że dieta bogata w witaminy ma wpływ na stan siatkówki oka. W szczególności zielone warzywa, takie jak m.in. szpinak, kapusta (uwaga - o warzywach i owocach można przeczytać wiele informacji na stronie RETINA FORUM, m.in. w dziale Na Zdrowie) mają ważny wpływ na plamkę żółtą w siatkówce oka, która jest punktem najostrzejszego widzenia. To zaledwie jeden milimetr kwadratowy, niewielki obszar siatkówki, gdzie światłoczułe komórki są położone bardzo blisko siebie. Dr Pauleikhoff wyjaśnił: "Jeśli spożywany w codzienne diecie te cenne barwniki w wystarczającej ilości, gromadzą się one w siatkówce i chronią je jak naturalne okulary tak skutecznie, jak to możliwe przed uszkodzeniami. To skuteczny sposób opóźniania zmian w siatkówce związanych z wiekiem". Od czasu do czasu, trochę czerwonego wina dozwolone "Picie jednego lub dwóch kieliszków czerwonego wina na tydzień jest bardzo dobre dla zdrowia oczu" - dodaje dr Pauleikhoff. Czerwone wino, a także winogrona, maliny, morwy, śliwki i orzechy ziemne zawierają cenny składnik o nazwie resweratrol (uwaga RF - polecamy artykuł o tym niezwykłym składniku, KLIKNIJ). Substancja ta znajduje się głównie w skórce owoców.. Od kilku lat korzyści zdrowotne resweratrolu przypisuje się m.in. w spowolnieniu miażdżycy. Badania na myszach udowodniły wpływ resweratrolu na zapobieganie zmian patologicznych, przede wszystkim naczyń krwionośnych, w cukrzycowej chorobie siatkówki i mokrej formy zwyrodnienia plamki żółtej związanej z wiekiem (AMD). Nie palę Wszystkie te wnioski zostały uzyskane w badaniach na zwierzętach, nie potwierdzone w dużych randomizowanych badaniach klinicznych u ludzi, ale jest niemal pewne, że ww. sposoby są skuteczne w profilaktyce naszego wzroku. Trzeba do tego dodać bardzo istotny element - rzucenie palenia pomaga w utrzymaniu zdrowia, w tym oczu do starości. "Bo palacze mają znacznie zwiększone ryzyko rozwoju AMD, a nawet zaprzestanie palenia tytoniu w zdiagnozowaniu choroby w jednym oku, która może mieć wpływ na ryzyko utraty wzroku w drugim oku, jest pozytywne" - stwierdza dr Pauleikhoff. Opr. i tłum.: Piotr Stanisław Król źródła: Bundesverband der Augenärzte Deutschlands e.V. (BVA), PRO Retina e.V. Deutschland |
data publikacji - 14 stycznia 2014 r. Francuscy i brytyjscy naukowcy po raz pierwszy na świecie zastosowali nową terapię, która pomaga w leczeniu pacjentów cierpiących na chorobę Parkinsona. Dotyka ona miliony chorych na świecie. Terapia nie leczy przyczyn choroby Parkinsona, ale zmniejsza uciążliwości związane z jej objawami.  Polega ona na wstrzykiwaniu bezpośrednio do mózgu genu terapeutycznego korzystnie wpływającego na produkcję dopaminy, która jest neuroprzekaźnikiem. Choroba Parkinsona powoduje obumieranie produkujących ją neuronów, a w konsekwencji - sztywność i drżenie kończyn. Polega ona na wstrzykiwaniu bezpośrednio do mózgu genu terapeutycznego korzystnie wpływającego na produkcję dopaminy, która jest neuroprzekaźnikiem. Choroba Parkinsona powoduje obumieranie produkujących ją neuronów, a w konsekwencji - sztywność i drżenie kończyn.Profesor Stephane Palfi, szef neurochirurgii w szpitalu w Creteil pod Paryżem, gdzie przeprowadzono badania, powiedział, że udało się wpłynąć korzystnie na symptomy motoryczne związane z chorobą - zmniejszyć sztywność ciała, przywrócić możliwość ruchu. Pacjenci mogą chodzić, lepiej śpią, ponieważ w nocy mogą się przewracać z boku na bok, łatwiej wstaje im się z łóżka. W przeciwieństwie do leczenia tradycyjnego u pacjentów nie występują uboczne skutki neuropsychologiczne - nie mają halucynacji i nie uzależniają się od leków. Nowa metoda pozwala także na lepsze w skutkach leczenie pacjenta, gdyż może się to odbywać przez całą dobę - w dzień i w nocy. źródło: Interia.pl - Fakty |
związany z zastosowaniem grafenu data publikacji - 17 września 2013 r. Grafen może być niebezpieczny dla ludzi. W toku niedawnych badań okazało się, że materiał ten z łatwością dziurawi błony komórkowe, upośledzając prawidłowe funkcje komórek. 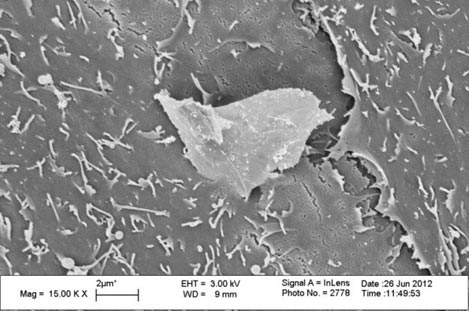 Fot.: Kawałek grafenu penetruje błonę komórkową keratynocytu Z dnia na dzień rośnie liczba potencjalnych zastosowań grafenu, przede wszystkim w elektronice i urządzeniach medycznych. Nadal nie wiadomo jednak, jak grafen działa na żywe komórki. Co stanie się, gdy dostanie się do organizmu podczas cyklu życiowego produktu? Z dnia na dzień rośnie liczba potencjalnych zastosowań grafenu, przede wszystkim w elektronice i urządzeniach medycznych. Nadal nie wiadomo jednak, jak grafen działa na żywe komórki. Co stanie się, gdy dostanie się do organizmu podczas cyklu życiowego produktu? - Nanomateriały mogą być celowo wstrzykiwane lub implantowane jako elementy nowych technologii biomedycznych. Nic więc dziwnego, że chcielibyśmy wiedzieć jak wygląda ich interakcja z organizmem człowieka - powiedział Robert Hurt, jeden z autorów badań. Biolodzy zauważyli, że grafen może samoistnie przedostawać się do komórek. Dzieje się tak tylko wtedy, gdy od arkuszy materiału odrywają się mniejsze, ostro zakończone formy. Mikrokawałki z wypustkami z łatwością perforują błony komórkowe. Komputerowe symulacje zostały potwierdzone w praktyce. Zespół naukowy Annette von dem Bussche umieścił na szalce Petriego z nanoarkuszami grafenu ludzkie komórki płuc, skóry i układu immunologicznego. Obserwując mikrośrodowisko mikroskopem elektronowym jednoznacznie wykazano, że grafen dostawał się do komórek. Dziurawiące błony kawałki były stosunkowo duże, bo aż 10-mikrometrowe. Teraz naukowcy będą pracować nad metodami zabezpieczającymi wnikanie grafenu do żywych komórek. W przeciwnym wypadku, trzeba będzie wstrzymać badania nad grafenem wykorzystywanym w nanotechnologiach biomedycznych. Więcej na temat nanotechnologii w medycynie na portalu Interia.pl źródło: Interia.pl - NT Nowe technologie |
data publikacji - 21 marca 2013 r. Na pocztę kontaktową strony Retiny Forum skierowano w ostatnim czasie pytania dot. szansy skutecznej terapii w chorobie zwanej wrodzoną ślepotą Lebera (Leber congenital amaurosis - LCA). [uwaga: LCA jest często mylona z LHON; w przypisie na końcu artykułu wyjaśnienie prof. Macieja Krawczyńskiego]  Informujemy, że kilka lat temu doniesiono w prasie o zastosowaniu eksperymentalnej terapii genowej, w której pewien Kanadyjczyk dotknięty tą chorobą odzyskał częściowo zdolność widzenia. Kilkanaście miesięcy później lekarze poinformowali, że terapia została zastosowana u kolejnych trzech osób. Informujemy, że kilka lat temu doniesiono w prasie o zastosowaniu eksperymentalnej terapii genowej, w której pewien Kanadyjczyk dotknięty tą chorobą odzyskał częściowo zdolność widzenia. Kilkanaście miesięcy później lekarze poinformowali, że terapia została zastosowana u kolejnych trzech osób.LCA upośledza wzrok u najmłodszych dzieci z powodu uszkodzenia genu RPE65. Gen ten produkuje specjalny rodzaj witaminy A, by komórki siatkówki mogły prawidłowo odbierać światło. W styczniu 2008 r. lekarze wszczepili wspomnianemu na początku pacjentowi miliony kopii nieuszkodzonego genu RPE65. Pacjent stwierdził prawie natychmiastową poprawę wzroku. Rok później lekarze w jednym z raportów opublikowanych w „New England Journal of Medicine” donoszą, że wzrok trzech ochotników nie pogorszył się. Nie było też niesprzyjających reakcji organizmu. - Po roku terapia z wykorzystaniem genu RPE65 okazała się bezpieczna i prowadzi do stabilnej poprawy wzroku - powiedział doktor Artur V. Cideciyan, który prowadzi badania. Jedna z pacjentek powiedziała, że w wyniku tej terapii nauczyła się ona po roku odczytywać zegar na desce rozdzielczej samochodu swoich rodziców. Naukowcy odkryli, że pacjentka dostrzega światło, wykorzystując do tego część oka, do której wstrzyknięto jej zdrowe DNA. Jej wzrok poprawił się, ponieważ mózg nauczył się wykorzystywać informacje otrzymywane z tego fragmentu oka. Doktor Paul A. Sieving, dyrektor National Institutes of Health' National Eye Institute uważa te badania za rewolucyjne: Rezultaty leczenia są bardzo znaczące, jest to pierwszy krok do wykorzystania terapii genowej w leczeniu osób tracących wzrok. Uważam, że kwestią czasu jest tylko to, aby ta technika była wykorzystywana w leczeniu innych chorób genetycznych. Obecnie oczekujemy, także i w Polsce, na wprowadzenie w szerokim zakresie tej terapii w chorobie LCA, która dotyka niemowlęta, tuż po urodzeniu. Jeszcze niedawno była uznawana za nieuleczalną, bez żadnych pozytywnych rokowań. Obecnie otwierają się możliwości, a wraz z nimi nadzieja na otwarcie oczu naszym dzieciom. źródło: Ctv.ca PRZYPIS: Fragment wywiadu Tomasza Wojakowskiego z prof. dr. hab. n. med. Maciejem Krawczyńskim: „Neuropatia Lebera" (wyjaśnienie dot. m.in. trzech różnych chorób z tym samym nazwiskiem: „Leber" w nazwie) Tomasz Wojakowski: Czy choroba Lebera jest prawidłową, zamienną nazwą neuropatii Lebera? Prof. Maciej Krawczyńśki (przyp. autora - podczas wywiadu dr M. Krawczyński nie miał jeszcze tytułu profesora, zostało to w tym miejscu uaktualnione): Choroba Lebera jest nazwą bardzo nieprecyzyjną i nie opisuje konkretnej jednostki chorobowej. W okulistyce bowiem są trzy różne jednostki chorobowe, które noszą nazwę od nazwiska swojego odkrywcy - niemieckiego okulisty Lebera i nieustannie mylone, zwłaszcza dwie z nich, które są genetycznie uwarunkowane. Pierwsza z nich jest określana dziedziczną neuropatią nerwów wzrokowych Lebera i tak powinna być nazywana (ang. Skrót LHON). Natomiast druga genetycznie uwarunkowana choroba, która z tą nie ma nic wspólnego, choć niezwykle często jest mylona to wrodzona ślepota Lebera (Leber congenital amaurosis - LCA). Wymagają one bezwzględnego rozróżnienia, ponieważ mają zupełnie inny charakter, inny wiek rozpoczęcia, inne struktury w oku chorują, inne możliwości postępowania itd. [...] Źródło: Otwórz oczy - www.otworzoczy.pl |
data publikacji - 16 marca 2013 r. Indukowane pluripotencjalne komórki macierzyste (komórki iPS; ang. iPSC - induced pluripotent stem cells) mogą być w przyszłości wykorzystane także w terapii degeneracji plamki żółtej związanej z wiekiem (AMD) - informacja ta jest w ostatnim czasie (początek 2013 roku) szeroko publikowana. 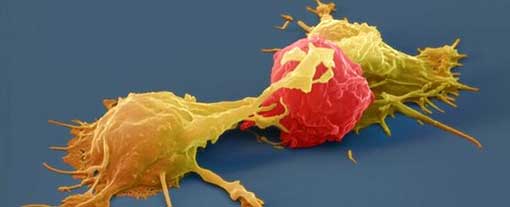 Na zdjęciu widoczne są limfocyty atakujące zaznaczoną na czerwono komórkę nowotworową. (fot. Eastnews/SPL) Jest to kolejny krok w wykorzystaniu tej bardzo obiecującej metody terapeutycznej. Inauguracją były podjęte po raz pierwszy badania, w których udało się stworzyć komórki, które skutecznie niszczą nowotwory i - co najważniejsze - mogą być bezpiecznie podane pacjentom chorym na raka. Tego przełomowego odkrycia dokonali japońscy naukowcy, pracujący pod kierownictwem Hiroshi Kawamoto w instytucie badawczym RIKEN. IPS to komórki pozyskiwane poprzez przeprogramowanie dorosłych komórek organizmu. Przed około siedmiu laty udało się je pozyskać przez Shinya Yamanaka. Aktualnie japoński naukowiec zamierza po raz pierwszy zastosować je u siedmiu tracących wzrok pacjentów chorych na AMD.
Wg oficjalnych doniesień w tej fazie badań przewiduje się przede wszystkim wykazanie, że stosowanie iPS w chorobie AMD jest całkowicie bezpieczne, bez skutków ubocznych. Decyzja zezwalająca na przeprowadzenie tych badań doświadczalnych jest teraz w gestii Ministerstwa Zdrowia w Japonii. Przewiduje się jej ogłoszenie na jesieni 2013 roku. W oficjalnych publikacjach ostrzega się jednak przed zbytnim pośpiechem w stosowaniu tej nowatorskiej metody z wykorzystaniem indukowanych pluripotencjalnie komórek macierzystych. Przypominana jest m.in. pierwsza terapia z wykorzystaniem komórek embrionalych w latach 90. ubiegłego wieku, gdy jeden z pacjentów, prawdopodobnie z powodu braku ostrożności w badaniach, zmarł w wyniku wstrząsu immunologicznego. Jednak dotychczasowe ustalenia wykazały, że stosowanie komórek iPS nie może prowadzić do aż tak poważnych skutków ubocznych, jak w przypadku transplantacji organów. Stosowana ma być tylko niewielka liczba komórek, a ich stan może być na bieżąco obserwowany i kontrolowany z zewnątrz przez soczewkę oka. W razie wystąpienia powikłań mogą być stosunkowo łatwo usunięte. Mało prawdopodobne wydaje się w tej metodzie terapeutycznej wystąpienie poważniejszych zagrożeń dla zdrowia i życia pacjenta. Jedno jest pewne, jest to prawdziwa, medyczna rewolucja w poszukiwaniu skutecznej terapii jednej z najpoważniejszych dzisiaj chorób oczu, degeneracji plamki żółtej oka związanej z wiekiem (AMD). Dotychczas stosowanie tej metody pozyskiwania komórek przynosiło bardzo dobre efekty w walce z rakiem. Przy okazji dostrzeżono nowy, bardzo ważny kierunek ratowania zdrowia. Siatkówka oka to jeden z najbardziej złożonych i skomplikowanych organów człowieka. Nie jest łatwo, ale można i tutaj dokonać niezwykłych rzeczy - w Japonii podjęto walkę, która może zaowocować wielkim sukcesem. Piotr Stanisław Król źródła: 1. Magazyn „Nature”: Stem cells cruise to clinic 2. www.heise.de/tp/blogs/3/99284 3. www.heise.de: Artikel 38/38701/1 4. odkrywcy.pl: Nowy sposób leczenia raka |
Komisja Europejska UE ogłosiła zwycięzców w konkursie Flagship. Dwa wybrane projekty badawcze są prowadzone z niemieckim udziałem. Jeden z projektów może mieć bardzo istotne znaczenie w technologii opracowywania implantu siatkówki oka. Projekt „Grafen” prowadzony pod kierunkiem Chalmers University of Technology w Szwecji ma być realizowany do 2020 roku w dotacji wysokości nawet do jednego miliarda euro.  „Grafen” jest cienką warstwą węgla grubości czystego atomu i należy do najtrwalszych i najbardziej odpornych warstw foliowych. Przewiduje się jego dwieście razy większą wytrzymałość na rozciąganie od stali, ma być również przezroczysty. Materiał ten ma umożliwić rewolucyjne zmiany w wielu dziedzinach, w tym np. w zastosowaniach medycznych, takich jak sztuczne siatkówki oczu. „Grafen” jest cienką warstwą węgla grubości czystego atomu i należy do najtrwalszych i najbardziej odpornych warstw foliowych. Przewiduje się jego dwieście razy większą wytrzymałość na rozciąganie od stali, ma być również przezroczysty. Materiał ten ma umożliwić rewolucyjne zmiany w wielu dziedzinach, w tym np. w zastosowaniach medycznych, takich jak sztuczne siatkówki oczu.Ze środków UE możliwe jest rozwinięcie współpracy interdyscyplinarnej w zakresie nowych technologii oraz urzeczywistnienie i umożliwienie zaangażowania się naukowców w realizacji ambitnych celów, długoterminowych badań. FET Flagship Initiative (FET - to przyszłość dla rozwoju nowych technologii) z Komisji Europejskiej jest bardzo ambitny, opierający się na szerokiej skali inicjatyw badawczych, wizjonerski w odniesieniu do nowych rozwiązań i szeroko zakrojonych innowacji technologicznych dla różnych zastosowań, mających docelowo przynieść wymierne korzyścią dla społeczeństwa. Szczegółowe informacje na temat sztandarowej inicjatywy można znaleźć na stronie internetowej CORDIS (Wspólnotowy Serwis Informacyjny Badań i Rozwoju): http://cordis.europa.eu/fp7/ict/programme/fet/flagship/ źródło: Ophthalmologische Nachrichten online, PRO Retina Deutschland UWAGA! Informacja dot. projektu opublikowana we wrześniu 2013 r.: Alarm dla technologii biomedycznych związany z zastosowaniem grafenu |
Odkrycie tegorocznych noblistów z medycyny otwiera drogę do tworzenia "części zamiennych" człowieka. Dzięki opracowanej przez nich procedurze można naprawiać np. zniszczone mięśnie serca. To jest gigantyczne odkrycie - powiedział genetyk prof. Piotr Stępień.  W poniedziałek (8.10.2012 r.) Nagrodę Nobla w dziedzinie medycyny i fizjologii otrzymali Brytyjczyk John B. Gurdon i Japończyk Shinya Yamanaka. Odkryli oni, że dojrzałe komórki organizmu można cofnąć w rozwoju do etapu komórek macierzystych, które potem są ponownie przekształcane w dowolne komórki organizmu. W poniedziałek (8.10.2012 r.) Nagrodę Nobla w dziedzinie medycyny i fizjologii otrzymali Brytyjczyk John B. Gurdon i Japończyk Shinya Yamanaka. Odkryli oni, że dojrzałe komórki organizmu można cofnąć w rozwoju do etapu komórek macierzystych, które potem są ponownie przekształcane w dowolne komórki organizmu.- To otwiera drogę do tworzenia części zamiennych człowieka, tych części, które nam się psują. Opracowaną przez nich procedurę można wykorzystać absolutnie do wszystkiego. Można naprawiać zniszczone mięśnie serca, można tworzyć nowe organy, można tworzyć nową nerkę. To zresztą już robiono na modelach zwierzęcych - powiedział prof. Piotr Stępień z Instytutu Biochemii i Biofizyki PAN oraz Instytutu Genetyki i Biotechnologii Uniwersytetu Warszawskiego. Podkreślił, że odkrycie omija problem wykorzystania komórek macierzystych, które dotychczas pobierano jedynie z embrionów. - To jest niezwykle istotne, bo dla wielu osób było to etycznie wątpliwe, a wręcz niedozwolone. Teraz wydaje się, że embriony przestały mieć jakiekolwiek znaczenie dla tworzenia komórek macierzystych - zaznaczył naukowiec. Jak wyjaśnił, odkrycie uczonych otwiera drogę do modyfikacji dorosłych komórek w ten sposób, że powstają z nich komórki macierzyste. - Nasze komórki zawierają komplet chromosomów, wszystkie zawierają pełną informację genetyczną, jednak wykorzystują tylko część tej informacji - powiedział. Właśnie dlatego komórki wątroby różnią się od komórek mięśni, bo używają tylko części genów. - Natomiast komórki macierzyste to komórki embrionalne, z których mogą powstać wszystkie możliwe komórki - tłumaczył genetyk. Odkrycie Yamanaki - wyjaśnił prof. Stępień - polega na tym, że za pomocą prostej procedury, czyli manipulacji czterema genami "te dorosłe komórki, które wydawałoby się, że na zawsze są skazane na bycie komórka mięśniową, komórką wątroby czy komórką skóry można odmłodzić". - Można cofnąć je w rozwoju do stanu embrionalnego. Stają się komórkami embrionalnymi do tego stopnia, że z tych komórek można było uzyskać żywe myszy - opisał rozmówca PAP. - Jest to coś zupełnie niezwykłego, coś co jeszcze wiele lat temu wydawało się mało możliwe. Okazało się, że plastyczność genów i fakt, że w każdej komórce mamy wszystkie geny pozwala na taką operację. Równie fascynujące jest to, że jest to procedura bardzo prosta - zaznaczył uczony. - Można pobrać odrobinę krwi człowieka, zastosować procedurę Yamanaki i po kilku dniach mamy komórki macierzyste. Z nich rozpoczynamy coś co nazywamy inżynierią tkankową - czyli budowanie organów". Jego zdaniem możliwości wykorzystania opracowanej procedury są nieograniczone. - Jednak jak zwykle w takich przypadkach zanim to się przełoży na konkretne procedury zaakceptowane przez środowisko medyczne, to jeszcze będzie trzeba trochę poczekać. Jeszcze nie ma konkretnych terapii, bo są w przygotowaniu - powiedział prof. Stępień. Zaznaczył, że ta nagroda jest wyjątkowa, bo na ogół Komitet Noblowski bardzo długo zwleka z przydzielaniem nagród, a tutaj od odkrycia upłynęło zaledwie kilka lat. "Gdy kilka lat temu przeczytałem ich pracę, byłem przekonany, że powinni otrzymać Nagrodę Nobla" - podkreślił uczony. źródło: PAP |
Substancję chemiczną, która przywraca widzenie, opracował międzynarodowy zespół badaczy. To brzmi jak scenariusz filmu science fiction - lek po wstrzyknięciu do oka przywraca widzenie na kilka godzin. Zdaniem naukowców z Uniwersytetu Kalifornijskiego w Berkeley oraz Uniwersytetu w Monachium to przełom w walce z najgroźniejszymi chorobami odbierającymi ludziom wzrok. Testy niezwykłego preparatu przeprowadzono na razie tylko na zwierzętach. Mechanizm działania jest jednak taki sam również u ludzi. Dlatego badacze uważają, że ich odkrycie pozwoli opracować skuteczną terapię również dla pacjentów cierpiących na zwyrodnienie barwnikowe siatkówki oraz zwyrodnienie plamki żółtej związane z wiekiem (AMD).Jak znieczulenie Choroby te są najczęstszymi przyczynami niedowidzenia lub ślepoty w krajach rozwiniętych. Choć ich przyczyny są różne, efekt jest ten sam - uszkodzenie komórek światłoczułych (fotoreceptorów) siatkówki. W rezultacie pole widzenia pacjentów stopniowo się zawęża. Opracowana przez naukowców substancja AAQ sprawia, że normalnie „ślepe” komórki siatkówki stają się światłoczułe. Jak tłumaczy prof. Richard Kramer z Uniwersytetu Kalifornijskiego, AAQ jest „przełącznikiem”, który przykleja się do komórek. Gdy padnie na nie światło, substancja ta powoduje przepływ jonów i aktywuje neurony. W taki sam sposób działają komórki siatkówki oka - czopki i pręciki. - Tak samo działają na przykład środki znieczulające. Przyklejają się do kanałów jonowych i pozostają tam przez pewien czas, sprawiając, że nic nie czujemy - mówi prof. Kramer. - Nasza cząsteczka jest inna, ponieważ aktywuje ją światło. Możemy ją uruchamiać i wyłączać światłem, a ona reguluje aktywność neuronów. - To ogromny postęp, jeśli chodzi o przywracanie widzenia chorym - mówi dr Russell Van Gelder, szef Wydziału Chorób Oczu w University of Washington w Seattle, który brał udział w badaniach. Opisuje je dzisiejsze wydanie fachowego pisma „Neuron”. Pierwsze eksperymenty z AAQ już przeprowadzono - na razie tylko na myszach. Wykorzystano specjalnie zmodyfikowaną genetycznie odmianę - myszki po kilku miesiącach po urodzeniu stawały się ślepe. Myszy boją się światła Naukowcy wstrzyknęli zwierzętom AAQ bezpośrednio do oka. Ich źrenice zaczęły się zwężać w reakcji na światło, co było sygnałem, że myszy ponownie zaczęły „widzieć”. Co więcej, myszy reagowały również na światło (unikały go), co świadczy o tym, że funkcje związane z interpretacją informacji działały. Przetestowana wersja leku z AAQ działa jedynie kilka godzin. Później - podobnie jak środki znieczulające - jest rozkładana i przestaje działać. - Najnowsze wersje tej substancji są lepsze, działają przez kilka dni, a nie przez kilka godzin - zapewnia prof. Kramer. Krótkie działanie AAQ wcale nie musi być wadą. Jak podkreślają naukowcy, dzięki temu jest to bezpieczniejszy sposób niż terapie genowe i zabiegi z wykorzystaniem komórek macierzystych. Z podawania leku można w każdej chwili zrezygnować. Nie zmienia też trwale struktury siatkówki. Sam zabieg jest też mniej inwazyjny niż modyfikacje genetyczne czy wykorzystanie elektronicznych implantów, które trzeba wszczepiać do ciała pacjenta. - Wielką zaletą tej metody jest to, że używamy zwykłej substancji chemicznej. Można zmienić dawkę, połączyć z innymi terapiami farmakologicznymi albo całkowicie ją porzucić, jeżeli nie jesteśmy zadowoleni z efektów - podkreśla prof. Kramer. - Kiedy opracujemy nowe cząsteczki chemiczne, zaoferujemy je do testowania pacjentom. Terapie polegające na modyfikacji genetycznej są trudne do odwrócenia, podobnie jak metody bazujące na elektronicznych czipach. Jest nadzieja Właśnie elektronika wszczepiana do oka jest obecnie najbardziej obiecującą formą terapii retinopatii barwnikowej. Opracowany przez niemiecką firmę Retina Implant AG czip ma 3 mm kw. i zawiera 1500 fotoreceptorów. Umieszczony w oku człowieka niewidomego częściowo przywraca wzrok. Inną metodą jest regeneracja siatkówki przy użyciu komórek macierzystych bądź wprowadzenie odpowiednich modyfikacji genetycznych do komórek oka za pomocą wirusów. Takie operacje już z powodzeniem przeprowadzono. źródło: Źródło: P. Kościelniak, Rzeczpospolita (Nauka) |
 Amerykańska Agencja ds. Żywności i Leków (FDA) ostrzega na swojej stronie internetowej pracowników amerykańskiej służby zdrowia o skupisku ciężkich zakażeń oczu, które miały miejsce w Miami na Florydzie, po wstrzyknięciu preparatu Avastin (bevacizumab) do gałki ocznej. Amerykańska Agencja ds. Żywności i Leków (FDA) ostrzega na swojej stronie internetowej pracowników amerykańskiej służby zdrowia o skupisku ciężkich zakażeń oczu, które miały miejsce w Miami na Florydzie, po wstrzyknięciu preparatu Avastin (bevacizumab) do gałki ocznej.O zakażeniach bakterią Streptococcus endophthalmitis w trzech placówkach medycznych, po użyciu preparatu Avastin, zawiadomił FDA Departament Zdrowia stanu Floryda. Powodem skażenia leku było przepakowanie jałowych, jednorazowych fiolek 100 mg/4 ml bez konserwantów do jednorazowych strzykawek o objętości 1 ml. Ustalono, że skażone ampułkostrzykawki pochodziły z jednej apteki znajdującej się w Hollywood na Florydzie. Apteka sprzedała następnie podzielony Avastin do różnych klinik okulistycznych w kraju. Jak dotąd FDA wie o przynajmniej dwunastu pacjentach z trzech klinik, u których wystąpiło ciężkie zakażenie oczu. Każdy z tych pacjentów cierpiał na zaburzenia wzroku przed wykonaniem zastrzyków preparatem Avastin. Niektórzy z nich utracili dotychczasowy procent zdolności widzenia z powodu zapalenia wnętrza gałki ocznej. FDA i władze stanu Floryda w dalszym ciągu badają przyczynę zakażeń. Śledztwo nie zostało jeszcze zakończone, jednak elementem łączącym wszystkie zakażenia jest apteka, w której dzielono Avastin na mniejsze dawki oraz jedna z przepakowanych partii preparatu Avastin. Agencja w wydanym komunikacie ostrzegła lekarzy o ryzyku wynikającym z przepakowywania oryginalnie zapakowanych, jałowych leków bez zachowania odpowiedniej techniki aseptycznej, co może negatywnie wpływać na jałowość produktu i stanowić potencjalne ryzyko zakażenia mikrobiologicznego. Agencja zachęca wszystkich lekarzy i pacjentów do zgłaszania wszelkich działań niepożądanych, skutków ubocznych lub jakichkolwiek innych zastrzeżeń po zastosowaniu preparatu Avastin w formie zastrzyków do gałki ocznej. źródło: oryginalna informacja dostępna na stronie: http://www.fda.gov/Drugs/DrugSafety/ucm270296.htm |
Amerykańscy naukowcy mogą sobie pogratulować. Udało im się odbudować uszkodzoną soczewkę w oku pacjenta, używając do tego komórek macierzystych pobranych ze... skóry. To nadzieja dla milionów niewidomych na całym świecie. Choroby siatkówki, takie jak: AMD, czyli zwyrodnienie plamki żółtej związane z wiekiem, retinopatia czy barwnikowe zwyrodnienie siatkówki, wreszcie będzie można pokonać. Taką nadzieję daje odkrycie naukowców z Schepens Eye Research Institute w Bostonie.  Badacze do eksperymentu użyli komórek skóry pobranych od specjalnych czerwonych laboratoryjnych myszek. Wybrali akurat taki rodzaj, aby łatwiej było śledzić im później aktywność czerwonych mysich komórek w oku. Przez ponad miesiąc przygotowywali je w laboratorium, traktując chemicznymi substancjami i zmuszając je do zamiany w komórki macierzyste. Następnie przeszczepili je do oka z uszkodzoną soczewką. Wynik przeszedł ich najśmielsze oczekiwania. Mysie komórki w cztery do sześciu tygodni przejęły funkcje komórek soczewki i uzupełniły ubytki w oku. Aby potwierdzić, czy działają jak należy, naukowcy przeprowadzili szereg testów. Uzyskane ze skóry komórki soczewki przeszły wszystkie badania bezbłędnie. Badacze do eksperymentu użyli komórek skóry pobranych od specjalnych czerwonych laboratoryjnych myszek. Wybrali akurat taki rodzaj, aby łatwiej było śledzić im później aktywność czerwonych mysich komórek w oku. Przez ponad miesiąc przygotowywali je w laboratorium, traktując chemicznymi substancjami i zmuszając je do zamiany w komórki macierzyste. Następnie przeszczepili je do oka z uszkodzoną soczewką. Wynik przeszedł ich najśmielsze oczekiwania. Mysie komórki w cztery do sześciu tygodni przejęły funkcje komórek soczewki i uzupełniły ubytki w oku. Aby potwierdzić, czy działają jak należy, naukowcy przeprowadzili szereg testów. Uzyskane ze skóry komórki soczewki przeszły wszystkie badania bezbłędnie.Zdaniem naukowców, metoda ta, po dopracowaniu, stanowi ogromną szansę przywrócenia wzroku pacjentom cierpiącym na najróżniejsze schorzenia siatkówki. źródło: Badania naukowców z Bostonu opublikowano w internetowym magazynie naukowym „Public Library of Science” („PLoS ONE”) |
W ostatnim czasie w niemieckich mediach pojawiły się informacje dotyczące podjęcia w USA badań klinicznych nad wpływem kwasu walproinowego* (opis leku wraz z ew. skutkami uboczmymi w przypisie, na końcu artykułu) na powstrzymanie postępu choroby genetycznej - zwyrodnienia barwnikowego siatkówki (RP). Temat ten wywołał ożywioną dyskusję, także i w Polsce, gdzie od kilku miesięcy prowadzony jest nabór ochotników do badań w jednej z klinik w naszym kraju. W połowie lipca na oficjalnej stronie Stowarzyszenia Pro Retina Deutschland e.V. zamieszczony został artykuł podsumowujący aktualny stan wiedzy na ten temat i zawierający ostrzeżenia przed pochopnym podejmowanie leczenia kwasem walproinowym barwnikowego zwyrodnienia siatkówki. Ochotnicy gotowi do testów klinicznych powinni mieć pełną wiedzę, co do skutków ubocznych stosowania tego leku i świadomie podejmować decyzję. Jak zaznaczono na stronie Pro Retina Deutschland e.V. nie jest łatwo stwierdzić w szybkim czasie działania pozytywnego i negatywnego danego leku w określonej chorobie Gdy są one przez pewien czas stosowane po zatwierdzeniu, może z czasem okazać się, że mają korzystny wpływ na inne choroby, dla których leki te nie zostały pierwotnie przewidziane. Takie obserwacje mogą skutkować nowym zastosowaniem leków. Jednakże ewentualne zastosowanie takiego leku w innym schorzeniu będzie tak samo poddane intensywnym badaniom pod względem efektów pożądanych i niepożądanych w celu określenia profilu ryzyka w stosowaniu w danej, konkretnej chorobie. Kwas walproinowy, stosowany od wielu lat w leczeniu padaczki, jest jednym z takich leków, który został poddany wstępnym badaniom klinicznym w zupełnie innej chorobie. W jednym z nich przez cztery miesiące poddano testom 13 pacjentów, u 7 stwierdzono poprawę stanu siatkówki. Wyciągnięto wstępne wyniki obserwacji sugerujące, że kwas walproinowy może mieć działanie ochronne, ale koniecznie wymaga to badań w zdecydowanie większym zakresie. Wyniki badań prowadzonych obecnie w USA nie są jeszcze dostępne. W szczególności, nie ma wyników w długotrwałym stosowaniu kwasu walproinowego. Jednakże są pojedyncze doniesienia sugerujące, że u pacjentów z padaczką mających zdrowe oczy, kwas walproinowy mógł spowodować ubytki w polu widzenia. Kwas walproinowy wpływa zatem być może na siatkówkę oka podobnie jak przeciwpadaczkowa vigabatryna; lek, który może doprowadzić do znacznego upośledzenia pola widzenia. Zrozumiałe są wątpliwość pacjentów, którzy z niecierpliwością czekają na skuteczny lek w ich konkretnej chorobie i pytają - po co przeprowadzane mają być nad nim badania testowe w tak długim czasie; czy nie można zacząć korzystać z już dostępnych na rynku leków? Otóż długie, dokładne badania kliniczne leków konieczne są z kilku bardzo ważnych powodów. Jest tylko domniemanie, że dany lek może pomóc w całkiem innej chorobie. Nieraz już bywało, że takie nadzieje oparte na podstawie obserwacji zaledwie kilku pacjentów, okazały się bezpodstawne. W tym konkretnym przypadku stosowanie kwasu walproinowego w retinitis pigmentosa miało pozytywny wpływ na pole widzenia u kilku pacjentów, co stwierdzono podczas niewielkiej liczby kontroli. Nie można wykluczyć zbiegu okoliczności. Potencjalnie korzystny wpływ zaobserwowano tylko na krótki czas. Ważne teraz jest, aby dowiedzieć się, w jakim stopniu przy długotrwałym stosowaniu lek ten będzie miał pozytywny, a w jakim ew. negatywny wpływ. Jak do tej pory nie ma wiedzy o odpowiednim dawkowaniu leku. Dawki tego samego leku mogą być bardzo zróżnicowane przy różnych zastosowaniach. Tego typu dane muszą być oficjalnie zatwierdzone. Zwłaszcza, gdy występują liczne działania niepożądane, jak ma to miejsce w wypadku kwasu walproinowego, takie jak: dysfunkcja i niewydolność wątroby, zaburzenia krwawienia, głuchota, zaburzenia czynności mózgu, aż do zaburzeń mózgu włącznie (demencja). Ostatnio organizacja zatwierdzająca leki w USA (FDA) ostrzegła przed podawaniem kwasu walproinowego w okresie ciąży, gdyż ma on negatywny wpływ na rozwój intelektualny dzieci i może prowadzić do niepożądanych zmian. Nie zaleca się stosowania walproinianu u kobiet w wieku rozrodczym; chyba, że w wyjątkowych sytuacjach potencjalnego zagrożenia śmiertelną chorobą. WAŻNE: Jeśli pacjent przyjmuje kwas walproinowy, ewentualne zaprzestanie brania tego leku powinno być konsultowane z lekarzem, gdyż nagłe odstawieniu wiąże.się ze znacznym ryzykiem! Podsumowując - należy stwierdzić, że długi okres wprowadzania danego leku z przeznaczeniem dla określonej choroby służy bezpieczeństwo pacjentów. Zdarza się, że nawet w badaniach o dużym zasięgu i długookresowych nie wykrywane są żadne negatywne skutki, a mogą one wystąpić w trakcie kolejnych wniosków dot. ich zastosowania. Skutki leczenia kwasem walproinowym barwnikowego zwyrodnienia siatkówki (retinitis pigmentosa) nie są dobrze poznane, zatem należy podchodzić do tego z ogromną ostrożnością. Decyzja należy do pacjentów, naszym obowiązkiem jest dostarczyć im jak najszerszej wiedzy w danym zakresie. Opracowanie: Piotr Stanisław Król źródło:
Przyspis: Co trzeba wiedzieć o leczeniu kwasem walproinowym? Kwas walproinowy jest jednym z podstawowych leków stosowanych w leczeniu padaczki, a także do leczenia ostrej manii, i jest stosowany w Stanach Zjednoczonych od 1978 roku. Chociaż środek ten nie jest zarejestrowany do leczenia profilaktycznego, jest również uznawany za lek normotymiczny pierwszego rzutu. Reakcja na leczenie. W wielu badaniach z kontrolą placebo wykazano, że kwas walproinowy jest skuteczny w leczeniu ostrych objawów maniakalnych, a pierwsze efekty kuracji obserwuje się w kilka dni po osiągnięciu stężenia w surowicy wynoszącego co najmniej 50 mg/L Objawy niepożądane/bezpieczeństwo. Podobnie, jak w przypadku litu, w materiałach dotyczących kwasu walproinowego i jego pochodnych FDA nakazała umieścić ostrzeżenie w czarnej ramce. Do potencjalnie śmiertelnych powikłań należą: niewydolność wątroby, działanie teratogenne (powodujące wady płodu), ostre krwotoczne zapalenie trzustki oraz bardzo rzadko obserwowane agranulocytoza i trombocytopenia (zmiany we krwi - zmniejszenie ilości granulocytów i płytek krwi). Te rzadkie i nagle występujące powikłania leczenia przy użyciu kwasu walproinowego wydają się być niezależne od dawki, tak więc rutynowe prowadzenie pomiarów stężenia leku we krwi niekoniecznie zmniejsza ryzyko ich wystąpienia. Mimo to zaleca się monitorowanie czynności wątroby i obrazu krwi co 6-12 miesięcy w celu ewentualnego wykrycia podwyższonego stężenia transaminaz, cech zapalenia trzustki oraz bardzo rzadko występujących agranulocytozy i trombocytopenii. Ostre zatrucie kwasem walproinowym charakteryzuje się przede wszystkim nadmierną sedacją oraz zaburzeniami procesów poznawczych. W przeciwieństwie do litu, nie ma określonego stężenia kwasu walproinowego w osoczu krwi, które wiąże się z występowaniem objawów zatrucia, chociaż klinicyści zgadzają się, że nie należy przekraczać poziomu 150 mg/L. Kwas walproinowy jest lekiem przeciwpadaczkowym, który w dużym stopniu wiąże się z białkami osocza, i u pacjentów z chorobami mogącymi wpływać na poziom albuminy wiążącej walproinian zaleca się oznaczanie poziomu wolnego kwasu walproinowego we krwi, a nie całkowitego stężenia tego środka. Na przykład, osoby z przewlekłymi chorobami wątroby i chorych z hipoalbuminemią (pacjenci z poparzeniami, w podeszłym wieku, w ciąży, z AIDS, itp.) powinny mieć oceniane stężenie wolnego leku we krwi. Stosunkowo często występującymi objawami niepożądanymi zależnymi od dawki są dolegliwości żołądkowo-jelitowe, nadmierna sedacja, wypadanie włosów i przyrost masy ciała. Smith i współpracownicy przeprowadzili analizę danych z badań klinicznych, i stwierdzili, że tolerancja leku poprawia się przy zastosowaniu postaci walproinianu sodu rozpuszczalnej w jelitach (enteric coated). Przy zastosowaniu tej odmiany leku obserwowano istotne zmniejszenie częstości występowania przyrostu masy ciała, drżenia, wypadania włosów oraz dolegliwości żołądkowo-jelitowych . Dolegliwości żołądkowo-jelitowe będzie można w przyszłości ograniczać przy zastosowaniu kapsułek zawierających walproinian w formie płynu (sprinkles), które będzie można dodawać bezpośrednio do jedzenia. Ogólnie rzecz ujmując, stosowanie mniejszej dawki leku wiąże się mniejszą częstością występowania objawów niepożądanych i lepszym profilem bezpieczeństwa terapii. Kwas walproinowy, tak jak wszystkie leki przeciwpadaczkowe, należy odstawiać powoli, gdyż nagłe odstawienie tego środka może być przyczyną wystąpienia napadów padaczkowych nawet u osób, u których takie napady w przeszłości nie występowały. Interakcje lekowe Jak już zaznaczono powyżej, kwas walproinowy wiąże się w dużym stopniu z białkami osocza i jest metabolizowany głównie w wątrobie, więc objawy zatrucia mogą wystąpić przy jednoczesnym zastosowaniu innego środka wiążącego się silnie z białkami lub/i metabolizowanego w wątrobie. Na przykład aspiryna, która również w dużym stopniu wiąże się z białkami osocza, może wypierać kwas walproinowy z jego miejsca wiązania z białkami, co może być powodem toksycznego działania wolnego walproinianu. Stężenie walproinianu we krwi może ulec znacznemu zmniejszeniu w przypadku zastosowania środków indukujących aktywność metaboliczną wątroby. Fluoksetyna może zwiększać stężenie kwasu walproinowego, gdyż hamuje metabolizm w wątrobie. Walproinian może znacznie zwiększać poziom lamotryginy w surowicy krwi i zwiększać ryzyko wystąpienia zagrażających życiu zmian skórnych w przypadku jednoczesnego stosowania tych środków. Ryzyko wystąpienia niewydolności wątroby ulega zwiększeniu przy stosowaniu kwasu walproinowego w skojarzeniu z innymi lekami przeciwpadaczkowymi. Współpraca w leczeniu W Stanach Zjednoczonych dostępnych jest pięć preparatów walproinianów do stosowania doustnego: kwas walproinowy, walproinian sodu, dwuwalproinian sodu, dwuwalproinian sodu o przedłużonym uwalnianiu (ER) oraz dwuwalproinian sodu w postaci kapsułek zawierających płyn, który można rozpuścić w jedzeniu (sprinkles). Są również dostępne postaci w czopkach i do stosowania dożylnego. Kwas walproinowy i walproinian sodu są szybko wchłaniane po podaniu doustnym. Największe stężenie w surowicy uzyskują po 2 godzinach od przyjęcia dawki. Dwuwalproinian sodu - postać rozpuszczalna w jelitach, zawierająca takie same ilości kwasu walproinowego i walproinianu sodu - uzyskuje największe stężenie we krwi w 3-8 godzin po podaniu doustnym. W przypadku stosowania postaci w kapsułkach do rozgniatania, zawierających płynną postać leku (sprinkles) nawet jeszcze później, szczególnie przy rozpuszczeniu leku w żywności. Wszystkie preparaty do stosowania doustnego, poza postacią ER, powinno się przyjmować dwa razy na dobę jeśli zalecana dawka przekracza 250 mg/d . Postać diwalproinianu o przedłużonym uwalnianiu (ER) można stosować raz na dobę, gdyż w przypadku tej formuły substancja czynna uwalnia się z preparatu ze stałą prędkością przez ponad 18 godzin. Ponieważ preparat ten można stosować raz dziennie, i charakteryzuje się lepszym, niż klasyczne formuły, profilem tolerancji, to stosowanie diwalproinianu sodu ER może poprawić współpracę chorego w leczeniu. Przy zmianie preparatu na formę ER należy zwiększyć pojedynczą dawkę o 8-20% w celu kompensacji zmniejszenia całkowitej dobowej dawki leku. Treść przypisu na podst. art. Anny Lembke, Optimal Dosing of Lithium, Valproic Acid, and Lamotrigine in the Treatment of Mood Disorders , Primary Psychiatry. 2009;16(10):37-42; za zgodą tłumacza dr hab. n. med. Łukasza Święcickiego. źródło: http://www.dwubiegunowa.net.pl/artykul.php?ks=75 |
Naukowcy poinformowali o wyhodowaniu części oka w warunkach laboratoryjnych. To przełom w medycynie regeneratywnej, piszą autorzy badań w prestiżowym tygodniku „Nature”. Japońscy badacze posłużyli się komórkami macierzystymi. Pobudzili je do przekształcania się w komórki siatkówki: części oka odpowiadającej za odbiór bodźców wzrokowych. To, zdaniem komentatora Robina Alley'a z londyńskiego uniwersytetu UCL - jest dokonaniem wyjątkowym. - To jest złożona tkanka ze skomplikowaną strukturą. Siatkówka oka ssaków ma wiele warstw, niektóre są zrobione z komórek nerwowych inne nie, więc to jest wybitne osiągnięcie - mówi Alley. Do tej pory komórki macierzyste uważano za potencjalne źródło odtwarzania tkanek zrobionych z tylko jednego rodzaju komórek: wątroby,mięśni czy serca. Teraz rozpoczną się badania nad tworzeniem bardziej złożonych struktur. Japońscy naukowcy mają nadzieję, że ich osiągnięcie pomoże przywrócić wzrok wielu ludziom przez wyhodowanie i przeszczep zastępczej siatkówki. Wyhodowanie całego oka jest jednak jeszcze kwestią dalekiej przyszłości. Do eksperymentu wykorzystano komórki pluripotentne, czyli komórki macierzyste niepochodzące z ludzkich embrionów. Prace z tego rodzaju komórkami nie wzbudzają większych kontrowersji etycznych. Autorem badań jest Yoshiki Sasai z CentrumBiologii Rozwojowej RIKEN w Kobe. źródło: Nature / iar |
Udało się poznać przyczyny suchej postaci zwyrodnienia plamki żółtej (AMD), choroby która jest jedną z głównych przyczyn utraty wzroku na świecie - informuje „Nature”. Po roku 2020 około 7,5 miliona starszych osób może stracić wzrok z powodu zwyrodnienie plamki żółtej (AMD). W przebiegu AMD przeciekające naczynia krwionośne, odczyn zapalny oraz tworzenie nowych, nieprawidłowych naczyń prowadzą do uszkodzenia plamki żółtej - centralnej części siatkówki, odpowiedzialnej za ostre widzenie. To najczęstsza przyczyna ślepoty po 65. roku życia. Na ciężką postać AMD co roku zapada w Polsce 20 tys. osób. Po 50. roku życia na AMD zapada jedna osoba na 50, po 85. - jedna na 5. Pacjenci z AMD wymagają pomocy w codziennych czynnościach. Nie mogą czytać, prowadzić samochodu, nie rozpoznają twarzy mijanych osób. Zespół doktora Jayakrishny Ambati z University of Kentucky (USA) odkrył, że przyczyną najbardziej rozpowszechnionej "suchej" postaci AMD jest zmniejszona aktywność enzymu DICER1 w siatkówce oka. Myszy, u których wyłączono gen odpowiedzialny za wytwarzanie enzymu miały oczy uszkodzone w sposób odpowiadający AMD. Jak się później okazało, enzym DICER1 jest niezbędny do niszczenia małych fragmentów materiału genetycznego, zwanych Alu RNA. Gdy zabraknie enzymu, gromadzące się Alu RNA powoduje obumieranie komórek siatkówki. Dalsze prace mogą doprowadzić do opracowania skutecznych metod leczenia choroby - na przykład zwiększania wytwarzania DICER1 lub neutralizacji Alu RNA. Na razie ogromne znaczenie ma profilaktyka. Rozwojowi AMD sprzyja nadciśnienie, palenie tytoniu i ostre światło (dlatego dobrze jest nosić ciemne okulary). Krewni chorych na AMD także chorują częściej. Świeże powietrze, dieta bogata w warzywa i owoce, a także preparaty witaminowe, selen i cynk mają działanie ochronne. Jak ważna jest właściwa dieta, świadczy przykład Japonii - gdy po II wojnie światowej tradycyjny zdrowy sposób odżywiania zastąpiły tam amerykańskie fast foody, zachorowalność na AMD znacznie wzrosła. Działanie ochronne mają też takie substancje, jak luteina krystaliczna, dostępna w formie odpowiednich preparatów. Regularne wizyty u okulisty, zwłaszcza w starszym wieku, pozwalają w porę wychwycić początek choroby. Dobrą okazją jest konieczność dopasowania nowych okularów. Nawet nieznaczny spadek ostrości wzroku może bowiem wskazywać na rozpoczynające się zwyrodnienie plamki - lub inną patologię. Można samemu kontrolować wzrok przy pomocy tak zwanej siatki Amslera - kartki papieru z narysowaną kratką. Patrząc na nią chorzy widzą zniekształcenia linii, a w zaawansowanym stadium choroby w polu widzenia pojawia się ciemna plama. Do dokładnej diagnostyki służy badanie dna oka, tomografia optyczna, a także badanie siatkówki perymetrem plamkowym. źródło: TSz/PAP |
Tak zatytułowana została wiadomość opublikowana w dniu 11 stycznia 2011 roku w Ärzteblatt Online. Wyniki badań przeprowadzonych w USA: 6,5 procent obywateli tego kraju w wieku powyżej 40 lat choruje na zwyrodnienie plamki żółtej związane z wiekiem (AMD). Jak informują naukowcy z Madison, ilość zachorowań w przeciągu 15 lat znacznie zmniejszyła się. W badaniach przeprowadzanych w latach 1988-1994 poziom zachorowalności na AMD wynosił 9,4 procenta.  Według naukowców spadek ten jest wynikiem poprawy zdrowia społeczeństwa, którego podstawą są: ograniczenie ilości osób palących, zdrowa dieta, aktywność fizyczna i skuteczniejsze obniżanie ciśnienia krwi. Te właśnie czynniki mają zdecydowany wpływ na zwyrodnienie plamki żółtej związanej z wiekiem. Według naukowców spadek ten jest wynikiem poprawy zdrowia społeczeństwa, którego podstawą są: ograniczenie ilości osób palących, zdrowa dieta, aktywność fizyczna i skuteczniejsze obniżanie ciśnienia krwi. Te właśnie czynniki mają zdecydowany wpływ na zwyrodnienie plamki żółtej związanej z wiekiem.„Palenie jest szkodliwe dla oczu” Potwierdza tą tezę DOG - Deutsche Ophthalmologische Gesellschaft (Niemieckie Towarzystwo Okulistyczne). Papierosy i zmiany genetyczne mają wpływ ma chorobę siatkówki AMD. W Niemczech aktualnie około 4,5 mln. osób cierpi na tę chorobę, która w krajach uprzemysłowionych jest obecnie najczęstszą przyczyną utraty wzroku w populacji osób starszych. Największym czynnikiem ryzyka jest palenie tytoniu. Także uwarunkowania genetyczne, jak wynika z ostatnich badań, mogą odgrywać znaczącą rolę w rozwoju choroby i jej postępie. Niemieckie Towarzystwo Okulistyczne (DOG) podkreśla, jak ważna jest wczesna profilaktyka. Decydujący wpływ wieku w zachorowalności na AMD Zagrożonych wystąpieniem wczesnego stadium AMD w wieku od 65 do 74 lat jest ok. 15 procent osób, podczas gdy powyżej 85 roku życia już 1/3 populacji. „Jest prawdopodobne, że za dziesięć lat ponad milion osób w Niemczech będzie chorować na AMD w zaawansowanym stadium” - przewiduje rzecznik DOG, Profesor dr Christian Ohrloff. „U tych pacjentów może nastąpić ogromne ograniczenie jakości życia i całkowita utrata wzroku” - powiedział dyrektor Uniwersyteckiej Kliniki Okulistycznej we Frankfurcie nad Menem. Choroba jest podstępna Osoby dotknięte tym schodzeniem początkowo nie zdają sobie sprawy z niebezpiecznych procesów, jakie zachodzą w ich oczach - biało-żółte osady w komórkach, zwane druzami, zmiany w sieci i naczyniówki. W ciężkich przypadkach, w tzw. „mokrej” odmianie AMD, następuje przenikanie płynu tkankowego i krwi do siatkówki. Pacjent doświadcza drastycznego ograniczenia widzenia, a nawet dochodzi do całkowitej utraty wzroku. Palacze są szczególnie zagrożeni Ta grupa ryzyka ma zmniejszoną ilość witamin w organizmie, zwiększoną ilość wolnych rodników, które w dłuższym okresie czasu bezlitośnie atakują tkanki. Niemieckie Towarzystwo Okulistyczne (DOG) zaleca więc lekarzom w przypadku zdiagnozowania pierwszych objawów AMD natychmiastowe zalecenie pacjentowi: „Rzucić palenie!”. Wyniki badań pokazują, że witaminy: A, C, E, cynk i miedź, zmniejszają ryzyko rozwoju zaawansowanych postaci choroby o 25 proc. Luteina i zeaksantyna, karotenoidy także mają pozytywny wpływ na hamowanie postępu choroby. „Należy jednak brać pod uwagę, że nieodpowiednie dawki mikroelementów mogą zwiększać ryzyko zachorowania na raka - zwłaszcza u palaczy” - ostrzega ekspert DOG, Profesor dr Gary Lang z Uniwersytetu w Ulm. Ponadto koniecznie należy, w porozumieniu z lekarzem, regulować dawki cynku. Dziedziczna predyspozycja w AMD Wiele ostatnich badań potwierdza związek między zwyrodnieniem plamki żółtej i dziedzicznym uwarunkowaniem. Niektóre geny, które są odpowiedzialne za stany zapalne, odgrywają tutaj kluczową rolę. Wiedza o genetycznych czynników ryzyka może w przyszłości pomóc w ocenie poszczególnych procesów chorobowych i w określaniu grup ryzyka. Współdziałanie tych czynników genetycznych wraz z paleniem prowadzi do znacznego wzrostu ryzyka zachorowania na AMD. Cele przyszłych badań „Ponieważ zmiany demograficzne mogą wpływać na wzrost liczby osób dotkniętych AMD (co będzie miało znaczny wpływ na ekonomikę zdrowia), badania naukowe powinny zmierzać do opóźniania wystąpienia zwyrodnienia plamki żółtej, a nawet jej zapobieżenia” - powiedział dr Christian Ohrloff. W kolejnych badaniach należy poszerzać naszą wiedzę na temat specyficznych czynników środowiskowych w powiązaniu z ryzykiem uwarunkowań genetycznych i ich wpływu na rozwój tej choroby. Źródła: Ärztezeitung Online Pressemitteilung der DOG M. Dietzel, A. Farwick, H.-W. Hense: Genetik und Risikofaktoren der exsudativen AMD. In: Der Ophtalmologe, 2010, Vol. 107: 1103-1108 |
 Wystarczy zwiększyć poziom enzymu, który pomaga neuronom w komunikacji. Do jego obniżenia dochodzi pod wpływem odkładania się w mózgu tzw. blaszek starczych. Ich obecność jest znamienna dla alzheimera. Wystarczy zwiększyć poziom enzymu, który pomaga neuronom w komunikacji. Do jego obniżenia dochodzi pod wpływem odkładania się w mózgu tzw. blaszek starczych. Ich obecność jest znamienna dla alzheimera.Naukowcom z Instytutu Chorób Neurologicznych Gladstone'a w San Francisco udało się złagodzić przebieg choroby i zapobiec pojawieniu się jej najbardziej srogich oznak. Dokonali tego u gryzoni. Jak przyznaje kierownik zespołu dr Lennart Mucke, uczeni są podekscytowani wynikami swoich badań. Mogą one oznaczać znalezienie nowej strategii walki z demencją. Informuje o tym "Nature". W eksperymentach wykorzystali myszy zmodyfikowane genetycznie. W obszarach ich mózgów odpowiedzialnych za pamięć obniżyli poziom enzymu o nazwie EphB2. Uzyskali warunki, jakie mają miejsce w mózgach ludzi z alzheimerem. - Najbardziej ciekawiło nas, czy unormowanie poziomu enzymu doprowadzi do naprawy zaburzeń pamięci - relacjonuje dr Moustapha Cisse, główny autor pracy. - Byliśmy zachwyceni, gdy tak się stało. Naukowcy odkryli także, że blaszki starcze wiążą się z EphB2, co powoduje degradację enzymu. To tłumaczy, dlaczego u chorych obserwuje się obniżenie jego poziomu. - Zablokowanie tych wiązań i jednoczesne zwiększenie ilości EphB2 może być skutecznym celem terapeutycznym - uważa dr Mucke. Źródło: Izabela Filc Redlińska - "Rzeczpospolita" |
Amerykańska Agencja ds. Żywności i Leków (US FDA - US Food and Drug Administration) wydała zezwolenie na przeprowadzenie badań z wykorzystaniem komórek macierzystych u pacjentów z chorobą Stargardta  US FDA zatwierdziła metodę badań z wykorzystaniem komórek macierzystych w terapii u pacjentów z chorobą Stargardta. Ta choroba oczu jest rzadką formą zwyrodnienia plamki żółtej, która jest dziedziczona i rozpoczyna się w okresie dojrzewania lub wczesnej dorosłości. W Polsce prawdopodobnie dotkniętych tym schorzeniem jest ok. 4000 osób. Jak dotąd nie ma skutecznego sposobu, aby zatrzymać postęp choroby. US FDA zatwierdziła metodę badań z wykorzystaniem komórek macierzystych w terapii u pacjentów z chorobą Stargardta. Ta choroba oczu jest rzadką formą zwyrodnienia plamki żółtej, która jest dziedziczona i rozpoczyna się w okresie dojrzewania lub wczesnej dorosłości. W Polsce prawdopodobnie dotkniętych tym schorzeniem jest ok. 4000 osób. Jak dotąd nie ma skutecznego sposobu, aby zatrzymać postęp choroby.Firma biotechnologiczna Advanced Cell Technology (ACT) planuje przeprowadzenie badań z wykorzystaniem komórek macierzystych na dwunastu pacjentach. Przyczyną utraty wzroku w chorobie Stargardta jest ubytek fotoreceptorów, co z kolei wiąże się z degeneracją tzw nabłonka barwnikowego siatkówki (RPE). - „W laboratorium wykorzystujemy zarodkowe komórki macierzyste do hodowli zdrowych komórek nabłonka barwnikowego w celu wykorzystania ich w chorobie Stargardta oraz innych w formach dystrofii plamki żółtej oka” - powiedział dr Robert Lanza, dyrektor medyczny ACT. Zdrowe komórki mają być wstrzykiwane pacjentom do oka w celu powstrzymania fotoreceptorów przed dalszym procesem degeneracji. Zgodnie z ustawą metoda ta była zastosowana w badaniach na modelach zwierzęcych (szczury i myszy).Jej wyniki rokują duże nadzieje w terapii u ludzi. - „Mamy nadzieję na osiągnięcie podobnych korzyści terapeutycznych u pacjentów z różnymi formami chorób plamki żółtej oka” - stwierdził dr Lanza. Kliniczne badania fazy I i II prowadzone są w kilku ośrodkach medycznych w Stanach Zjednoczonych na 12 pacjentach z chorobą Stargardta w zaawansowanym stadium choroby. Celem testów jest dokładna analiza bezpieczeństwa i tolerancji komórek RPE po przeprowadzeniu transplantacji podsiatkówkowej. Czy metoda ta będzie skuteczna u ludzi - potwierdzić będą to musiały kolejne badania. Źródła: Advanced Cell Technology; Newsletter Deutsches Ärzteblatt z 22.11.2010 (Część 2); Spiegel online - Nauka |
 Na pierwszy rzut oka wyglądają jak zwykłe szkła kontaktowe. Ale to tylko pozory. Biosyntetyczne rogówki wykonane z kolagenu potrafią zdziałać cuda. U pierwszych pacjentów, którym je wszczepiono, doszło do regeneracji i naprawy uszkodzonej tkanki oraz poprawy widzenia. Informuje o tym "Science Translational Medicine". Na pierwszy rzut oka wyglądają jak zwykłe szkła kontaktowe. Ale to tylko pozory. Biosyntetyczne rogówki wykonane z kolagenu potrafią zdziałać cuda. U pierwszych pacjentów, którym je wszczepiono, doszło do regeneracji i naprawy uszkodzonej tkanki oraz poprawy widzenia. Informuje o tym "Science Translational Medicine".- Wyniki tych badań są ważne o tyle, że stanowią pierwszy dowód na możliwość zintegrowania się z ludzkim okiem rogówki, która została sztucznie stworzona - komentuje główna autorka prac, dr May Griffith z Ottawa Hospital Research Institute (zostały one przeprowadzone we współpracy z szwedzkim Linköping University). - Dzięki kolejnym badaniom, rozwiązanie to pomoże przywrócić wzrok milionom ludzi, dla których do tej pory jedyną nadzieją był przeszczep rogówki od dawcy. Rogówka jest cienką, przeźroczystą warstwą kolagenu, która spełnia dla gałki ocznej funkcję podobną do szyby okna. Aby światło mogło bez przeszkód wpadać do wnętrza oka, musi być ona całkowicie transparentna. Choroby, które prowadzą do jej "zabrudzenia" stanowią jedną z najczęstszych przyczyn utraty wzroku. Już ponad dekadę temu dr Griffith rozpoczęła prace nad wynalezieniem sztucznego zamiennika uszkodzonej rogówki. Został on stworzony z syntetycznego i rekombinowanego kolagenu. Współpraca ze szwedzkim chirurgiem okulistą, dr Perem Fagerholmem umożliwiła zastosowanie biosyntetycznych rogówek w praktyce. Dwa lata temu wszczepiono je 10 pacjentom ze Szwecji (tylko do jednego oka, po uprzednim usunięciu z niego chorego fragmentu). Uczeni zaobserwowali, że komórki i nerwy własnej rogówki pacjenta wrosły w implant. W rezultacie doszło do regeneracji tej warstwy oka. Co ważne, pacjenci nie musieli przyjmować leków immunosupresyjnych obniżających odporność, które stosuje się po tradycyjnym przeszczepie. Biosyntetyczna rogówka okazała się również wrażliwa na dotyk i nie stała na przeszkodzie w łzawieniu. Efekty? U sześciu osób doszło do poprawy widzenia (u dwóch nie zanotowano żadnych zmian, u reszty zaszły zmiany na gorsze). Były one na poziomie porównywalnym z tym, jaki uzyskuje się po transplantacji rogówki od dawcy. Źródła: rp.pl, Ottawa Hospital Research Institute |
przeciw retinopatii cukrzycowej i AMD
Naukowiec okulista - Rajendra Apte z Washington University School of Medicine w St. Louis prowadzi zaawansowane badania nad pozytywnym wpływem resweratrolu w terapii retinopatii cukrzycowej oraz AMD (zwyrodnienie plamki żółtej oka związane z wiekiem). Bardzo obiecujące wyniki badań na myszach doświadczalnych stwarzają realną nadzieję na skuteczne leczenie osób dotkniętych ww. chorobami. M.in. mówi się o szansie zastąpienia w leczeniu AMD preparatu Lucentis odpowiednio spreparowanym resweratrolem. Obniżyłoby to znacznie obecne koszty leczenia. Jak ostrożnie zaznacza naukowiec Rajendra Apte - preparat oparty na resweratrolu może okazać się także skuteczny w leczeniu retinopatii dziecięcej. Natomiast francuscy badacze z Centre National de la Recherche Scientifique dowiedli, że resweratrol obniża poziom cholesterolu, wpływa korzystnie na układ krążenia, zmniejsza ryzyko chorób nowotworowych. Do tych zalet dochodzi jeszcze jedna: hamuje łaknienie i nadmierne przybieranie na wadze. Obecnie trwają intensywne badania naukowe nad skuteczną walką z otyłością, która staje się powoli "cichym, podstępnym niszczycielem" w krajach wysokorozwiniętych, naszpikowanych fastfoodami, chipsami, "energetycznymi" napojami. Resweratrol z pewnością pomaga w zachowaniu zdrowej sylwetki i w walce ze złą przemianą materii. Póki co, preparaty medyczne preparatami, warto wzbogacać swoją codzienną dietę resweratrolem. W wypadku czerwonego wina, z umiarem. Jak ktoś nie może pić wina - winogrona ze skórką. Też dobre i skuteczne. |
w retinitis pigmentosa? W kwietniowym wydaniu „Archives of Ophthalmology” ukazał się artykuł, w którym znalazła się informacja o badaniach naukowych wykazujących, że w barwnikowym zwyrodnieniu siatkówki (retinitis pigmentosa) zażywanie zwiększonej ilości luteiny w połączeniu z witaminą A powoduje opóźnienie procesu utraty obwodowego pola widzenia. Jednocześnie nie potwierdzono poprawy widzenia centralnego (plamka żółta) u pacjentów, którzy otrzymali dodatkowo zwiększone dawki witaminy A wraz z luteiną, w porównaniu do tych pacjentów, którzy w tym czasie otrzymywali placebo. Wyniki wcześniej przeprowadzanych badań wykazały pozytywny wpływ luteiny na zmniejszenie ryzyka zaćmy i zwyrodnienia plamki żółtej. W ostatnio przeprowadzonych przez zespół dr. Eliot'a Berson'a z Harvard Medical School w Bostonie badaniach uczestniczyło w ciągu czterech lat 225 pacjentów z retinitis pigmentosa (niepalących, z „typową” formą RP). Codziennie otrzymywali oni oprócz 15.000 IE witaminy A - 12 g luteiny lub placebo. Ich celem było sprawdzenie, czy dodatkowe zażywanie luteiny ma pozytywny wpływ na widzenie centralne. Nie stwierdzono tego jednoznacznie, natomiast w grupie badanych pacjentów zażywających luteinę z witaminą A wykazano znacznie mniej degeneracji w widzeniu obwodowym. „Obwodowe pola widzenia jest ważne” - powiedział dr Berson w rozmowie z Reuters Health. - „Ten wtórny wynik końcowy badań należy traktować poważnie”. Mimo negatywnych komentarzy (jak to w nauce już bywa) w tym samym numerze „Archives of Ophthalmology” dr. Roberta Massof'a (Lions Vision Center z Baltimore) oraz dr. Geralda Fishman'a (University of Illinois z Chicago) dr Berson nie zgadza się z krytyką wyników badań i ripostuje - „Połączenie w diecie tłustych ryb, witaminy A oraz luteiny może prowadzić u niektórych pacjentów do przedłużenia nawet do 20 lat funkcji widzenia peryferyjnego, co w wielu przypadkach może powodować zachowanie wzroku do końca życia”. Redakcja RETINY FORUM na podstawie uważnych, własnych obserwacji dotychczas przeprowadzanych badań naukowych, a także (co ma istotne znaczenie) informacji Czytelników może w tym miejscu doradzić osobom dotkniętym barwnikowym zwyrodnieniem siatkówki - dietę bogatą w luteinę, zeaksantynę, witaminę A (tutaj należy zachować umiar, ze względu na negatywne działanie na metabolizm przy przedawkowaniu), tłuste ryby (np. makrela, śledź, łosoś) zawierające kwasy Omega 3, która ma zdecydowanie pozytywny wpływ na siatkówkę oka. Nie należy zapominać o ruchu fizycznym. Umiarkowany stres wynikający z aktywnego trybu życia ma, jak wykazały już badania naukowe, także pozytywny wpływ na zdrowie (również siatkówki oka). Źródła: „Archives of Ophthalmology”, „Pro Retina”, własne RF |
- możliwość zastosowania w implantach siatkówki oka Dr inż. Joachim Burghartz, dyrektor Instytutu Mikroelektroniki w Stuttgarcie i wykładowca na tamtejszym Uniwersytecie otrzymał nagrodę państwową za wkład w opracowanie technologii produkcji super-cienkiego chipu krzemowego. Chipy mogą znaleźć zastosowanie w dziedzinie mikroelektroniki, techniki mikrosystemów i technologii medycznych. Mogą także być wykorzystane do produkcji implantu siatkówki oka. Burghartz wraz ze swoim zespołem opracował nowoczesną metodę wytwarzania układów krzemowych, które są do 50 razy cieńsze od dotychczasowych. - „Cienkie chipy są jeszcze bardziej płaskie niż papier, bardzo elastyczne i nie kruszą się, mogą być laminowane tworzywem sztucznym” - oświadczył Burghartz. Doskonale nadają się do implantów siatkówki. Obecnie są testowane klinicznie na Uniwersytecie w Tybindze. Należy idealnie przystosować je do oka, powinny mieć dostosowany kształt, być odpowiednio uwypuklone - i nie mogą mieć ostrych krawędzi oraz narożników. Dla osób dotkniętych chorobami siatkówki jest to kolejna w ostatnich miesiącach, bardzo optymistyczna informacja. Wszystko wskazuje na to, że w całkiem niedługim już czasie bardzo wysokiej jakości implanty stworzą w dużej mierze możliwość odzyskania widzenia. Źródło: „Ophthalmologische Nachrichten online” |
Doświadczenie przeprowadzono na grupie 39.876 zdrowych kobiet, czynnych zawodowo, w wieku 45 lat lub więcej. Czas trwania badań trwał dziesięć lat. Co drugi dzień otrzymywały losowo 100 mg Aspiryny lub placebo. Po upływie tego okresu wyniki wykazały 111 przypadków wystąpienia AMD wśród osób biorących Aspirynę i 134 przypadki zachorowań wśród przyjmujących placebo. Zespół Williama G. Christen'a z Bostonu ustalił jednoznacznie, że niewielkie dawki kwasu acetylosalicylowego przyjmowanego regularnie, nawet w długim okresie czasu, nie szkodzą oraz nie mają także żadnego korzystnego wpływu profilaktycznego w przypadku tej choroby. Źródło: www.ophsource.org |
Preparaty: Bevacizumab (Avastin) i Ranibizumab (Lucentis) Badanie porównawcze przeprowadzone zostało w klinice Bostońskiej - 20 pacjentom wprowadzano do jednego oka: Lucentis (7) lub Avastin (13). W pierwszym etapie - w przeciągu trzech miesięcy jedną iniekcję, a następnie zastosowano zmienne dozowanie w zależności od wyników badań OCT. Badanie porównawcze dotyczyło ostrości widzenia oraz obrazu centralnej części siatkówki odpowiedzialnej za tę funkcję (Fovea). W wyniku badań porównawczych nie stwierdzono żadnych różnic w efektywnym oddziaływaniu obydwu preparatów. Trzeba jednak zaznaczyć, że w celu uzyskania pełnych, statystycznych wyników konieczne będzie przeprowadzenie badań na większej ilości pacjentów. Różnica podczas badań obydwu grup pacjentów dotyczyła ilości iniekcji: grupa "Lucentis" - przeciętnie 4 w przeciągu sześciu miesięcy; grupa "Avastin" - o jedną więcej (5 iniekcji). Obecnie trwają liczne badania naukowe (między innymi w Bremie- VIBERA Studie), których celem jest dokładne stwierdzenie różnic pomiędzy tymi dwoma lekami stosowanymi u pacjentów z AMD. źródło: American Journal of Ophthalmology, 2009 Ophthalmologische Nachrichten online PRO-Retina Deutschland e. V. OBJAŚNIENIE INFORMACJI: Avastin - w przeciwieństwie do preparatu Lucentis - nie został początkowo przeznaczony do leczenia wysiękowego AMD lecz do dożylnego leczenia onkologicznego raka okrężnicy i odbytnicy. W ostatnim czasie w wielu krajach (w tym i w Polsce) zaczęto jednak stosować w niektórych ośrodkach leczniczych Avastin w terapii degeneracji plamki żółtej związanej z wiekiem (AMD). Motywuje się to brakiem różnicy w działaniu obydwu preparatów oraz zdecydowanie niższymi kosztami. Kontrowersje wzbudziły jednak przypadki powikłań po iniekcji Avastinu u pacjentów z AMD (z tego, co mi wiadomo - w Niemczech oraz Kanadzie), które w niektórych przypadkach doprowadziły do całkowitej utraty widzenia w poddanym terapii oku. Wszystko wskazuje jednak na to, że przyczyna nie leżała w samym preparacie, lecz w kilkakrotnym dozowaniu leku z tego samego pojemnika kilku pacjentom. Mogło w tej sytuacji dojść do jego zanieczyszczenia i wynikających z tego powodu powikłań. Avastin jest przeznaczony, jak wyżej wspomniałem, do leczenia onkologicznego i iniekcji o wiele większych dawek niż ma to miejsce okulistyce - stąd duże pojemniki. Wszystko wskazuje na to, że Avastin - po stwierdzeniu identycznego oddziaływania jak Lucentis - zostanie wprowadzony do leczenia wysiękowego AMD, oczywiście rozprowadzany w odpowiednich, jednorazowych pojemnikach do iniekcji. Dla pacjentów jest to zapewne dobra wiadomość, ponieważ koszty leczenia tym preparatem są o wiele niższe niż Lucentisem. AMD jest obecnie najczęstszą przyczyną utraty wzroku w krajach wysokorozwiniętych, w których przeciętna długość życia ulega stałemu wydłużaniu. Ze względu na stan polskiej służby zdrowia i zubożenia naszego społeczeństwa, szczególnie ludzi w wieku emerytalnym, koszty leczenia tej choroby mają ogromne znaczenia. Tańszy lek o identycznym działaniu jest szansą na uratowanie zdrowia większej ilości pacjentów. Po ukazaniu się informacji m.in. o preparacie Avastin i przypadkach powikłań (prawdopodobne przyczyny jw.) do portalu RETINA FORUM przyszedł list jednego z pacjentów, który po kilkumiesięcznej terapii Avastinem w jednym z ośrodków w woj. łódzkim, w dużej mierze odzyskał ostrość widzenia i znacznie poprawił się stan jego siatkówki. Jak stwierdził: "na droższe leczenie nie byłoby mnie po prostu stać...". Sprawa jest z pewnością kontrowersyjna. Wielu chorych na AMD z niecierpliwością będzie oczekiwać na ostateczne, wiążące wyniki porównawczych badań klinicznych nad preparatami: Bevacizumab (Avastin) i Ranibizumab (Lucentis). Jeśli nie będzie między nimi żadnych różnic w terapii degeneracji plamki żółtej związanej z wiekiem - warto po prostu wybrać tańszą ofertę. |
Obiecujący, biologiczny rezultat badań z zastosowaniem rzęskowego czynnika neurotropowowego (CNTF) z aplikaturą NT-501 f-my NEUROTECH (USA) W badaniach bierze udział około 60. pacjentów z RP z wczesnym oraz późnym stadium rozwoju choroby, z zastosowaniem małych oraz zwiększonych dawek preparatu dozowanych do jednego oka. Po relatywnie krótkim czasie badań doświadczalnych wynoszącym 12. miesięcy nie można jeszcze u nich "mierzalnie" stwierdzić poprawy widzenia. Optymistyczny jest jednak już na tym etapie wyraźny, biologiczny efekt terapeutyczny, uwidaczniający się w siatkówce oka pacjentów. Badania są kontynuowane, przewidziany czas: 18. miesięcy w stanach zaawansowanych oraz 30. miesięcy we wcześniejszych. Jest więc nadzieja, że pozytywny biologiczny efekt badań przełoży się na poprawę wzroku u chorych na Retinitis Pigmentosa. Czym jest rzęskowy czynnik neurotropowy (ciliary neurotrophic factor - CNTF)? Udowodniono, że pewne czynniki neurotropowe mogą hamować utratę komórek fotoreceptorowych w procesie zwyrodnienia siatkówki. Jeden z nich, rzęskowy czynnik neurotropowy (CNTF), był skuteczny w ograniczeniu utraty widzenia spowodowanej przez śmierć fotoreceptorów w 13 modelach zwierzęcych indukowanego zwyrodnienia obwodowego siatkówki. CNTF przeszedł pomyślnie badania bezpieczeństwa fazy I oraz fazy II. Specjalnie dla tych celów, NEUROTECH (USA) opracowało technologię opłaszczenia komórkowego (encapsulated cell technology - ECT), którą zastosowano w aplikaturach NT-501, w których komórki są osłonięte przez półprzepuszczalny polimer zapewniający stopniowe uwalnianie CNTF. tłum. i opr.: Piotr Stanisław Król Źródło: www.neurotechusa.com/news_events/pr_2009-05-28.asp www.pro-retina.de |
Uwidaczniając ciemno zabarwione komórki pigmentowe, od których zależy stan zdrowia oka, można będzie o całe lata wcześniej rozpoznawać choroby degeneracyjne siatkówki - informuje pismo „Investigative Ophtalmology and Visual Science”. Zespołowi prof. Davida Williamsa z University of Rochester udało się po raz pierwszy obserwować żywe "ciemne komórki" w oku pacjenta. Dzięki takim obserwacjom można by na przykład przewidywać wystąpienie degeneracji plamki żółtej - jednej z najczęstszych przyczyn utraty wzroku - na wiele lat przed wystąpieniem objawów. Już w roku 1997 zespół Williamsa jako pierwszy na świecie obserwował indywidualne komórki światłoczułe siatkówki, posługując się techniką optyki adaptacyjnej - opracowaną pierwotnie przez astronomów, z myślą o zastosowaniu w obserwacji gwiazd. Teraz technika adaptacyjnej optyki została połączoną z metodą, dzięki której komórki RPE zaczęły świecić - oświetlano je słabym światłem o niebieskiej lub zielonej barwie. Źródło: PAP, „Investigative Ophtalmology and Visual Science” |
Odkrycie substancji stymulujących komórki Müllera do podziałów, a w konsekwencji do regeneracji siatkówki, przynosi nową nadzieję na terapię takich schorzeń, jak zwyrodnienie plamki żółtej czy retinopatia barwnikowa, często prowadzących do ślepot. Komórki Müllera zaobserwowano już stosunkowo dawno, początkowo jednak przypisywano im wyłącznie funkcję ochronną. W ciągu ostatnich lat wykazano, że mogą one podejmować cykl komórkowy, proliferować, a następnie różnicować się w niektóre typy komórek. Przejawiają więc charakter progenitorowy (komórki progenitorowe różnią się od komórek macierzystych zdolnością do szybkiej proliferacji i bardziej ograniczoną pulą komórek, do których mogą różnicować). Nie było jednak wiadomo, jak skłonić te z reguły "uśpione" komórki do takiego zachowania. Zbawiennym związkiem okazał się kwas glutaminowy oraz jego pochodna - kwas aminoadypinowy (ang. aminoadipate). Obie substancje wstrzyknięte do oka myszy wywoływały podziały i proliferację komórek Müllera. Aby sprawdzić, czy badane substancje różnią się swoim działaniem, dodano je do osobnych hodowli komórek in vitro, a następnie podano myszom. W obu przypadkach zaobserwowano proliferację komórek. Na uwagę zasługuje jednak fakt, że w przypadku komórek stymulowanych kwasem aminoadypinowym, były one zdolne do migracji do różnych miejsc w siatkówce i różnicowania się w odpowiednie typy komórek. Co najważniejsze dla terapii takich chorób, jak wspomniane na początku zwyrodnienie plamki żółtej czy retinopatia barwnikowa, stymulowane komórki wstrzyknięte pod siatkówkę potrafią różnicować się w wyspecjalizowane komórki fotoreceptorowe. To właśnie ich utrata jest odpowiedzialna za ślepotę, ich odtworzenie zatem mogłoby przywrócić pacjentom wzrok. Naturalnie badania takie od zastosowań klinicznych dzieli jeszcze długa droga. Pierwszym krokiem będzie sprawdzenie możliwości regeneracji uszkodzonych tkanek i przywrócenia wzroku na zwierzęcych modelach wspomnianych wyżej chorób. Prawdopodobnie do stymulacji komórek posłuży kwas aminoadypinowy, uznany za bezpieczniejszy niż glutaminian (ten ostatni, w wysokich dawkach, może wykazywać działania niepożądane). Niemniej jednak odkrycie to przynosi nadzieję na stosunkowo prostą terapię, być może nawet z użyciem własnych komórek pacjenta - można by je po prostu pobudzić do regeneracji uszkodzonych tkanek w oku chorego. Wyeliminowałoby to również konieczność przeszczepiania siatkówki lub komórek od dawcy, co jest zawsze związane z większym ryzykiem niż zastosowanie komórek autologicznych. ScienceDaily |
Komórki macierzyste sprawiły nam kolejną niespodziankę. Okazało się, że są także w oku. A to oznacza, że możliwe będzie leczenie wielu beznadziejnych obecnie przypadków ślepoty - pisało "Science" Wymiana zmętniałej (np. wskutek zaćmy) soczewki stała się rutynowym zabiegiem leczniczym. Gorzej z siatkówką. Jej uszkodzeń, zwanych retinopatiami, nie daje się leczyć. Możemy co najwyżej ograniczać ich skutki. A są one, niestety, dość częstą przyczyną utraty wzroku u chorych na tzw. genetyczne zwyrodnienie siatkówki (retinitis pigmentosa) oraz osób starszych, zwłaszcza cierpiących na cukrzycę czy nadciśnienie tętnicze. - Mamy nadzieję, że w ciągu paru lat retinopatie będą uleczalne - stwierdził Vincent Tropepe z uniwersytetu w Toronto. Jego zespół dokonał odkrycia tyleż przełomowego, ile zaskakującego. Wykazał, że oko ma potencjalną zdolność do regeneracji uszkodzonej siatkówki. Zdolność tę zawdzięcza komórkom macierzystym, a więc takim, które mogą przekształcić się w dowolną tkankę organizmu. Przypomnijmy, że niedawno tygodnik "Science" obwołał komórki macierzyste "naukowym przebojem minionego roku", argumentując to tym, że "potwierdzają pokładane w nich nadzieje". Jak się okazało, także w okulistyce. - Zachwyt nad nimi jest o tyle uzasadniony, że jako jedyne dzielą się przez całe życie i umożliwiają naprawę naszych zużywających się z dnia na dzień organizmów. Sęk w tym, że choć komórek takich pełno w naszych zarodkach, potem ostają się tylko w nielicznych miejscach, a głównie w szpiku. I wydawało się niemal pewne, że nie ma ich w naszej siatkówce. Okazuje się jednak, że są - zapewnia Tropepe. Jego zdaniem ludzie mają prawo cieszyć się z tego - dokonanego u myszy - odkrycia. - Wiadomo było, że mają je dorosłe płazy i ryby. Teraz wiemy, że mają je też dorosłe ssaki. Więc na 99 proc. także i ludzie - zaznacza. Niestety, u dorosłych ssaków komórki macierzyste siatkówki z niejasnych powodów są nieaktywne. - Najprawdopodobniej stoją za tym jakieś substancje, które blokują ich działanie - przypuszcza uczony. - Ale gdyby udało się przełamać ich opór... Tropepe jest optymistą. Uważa, że poznanie enzymów hamujących aktywność komórek macierzystych siatkówki umożliwi niechirurgiczne leczenie retinopatii. - Wystarczyłoby podać substancję, która odblokuje komórki macierzyste, i czekać, aż uszkodzona siatkówka zacznie się regenerować. A jeśli nie zacznie? - To pozostaje wariant awaryjny - nie daje za wygraną. - Rok temu moi koledzy z uniwersytetu w Wisconsin udowodnili, że komórki macierzyste dają się hodować w laboratorium. Skoro tak, to teoretycznie możliwe jest ich pobranie, namnożenie in vitro i powtórne wszczepienie pacjentowi. Zdaniem komentatorów w tym przypadku niewiele musi dzielić teorię od praktyki. - Na moje oko kilka lat - mówi prof. Derek van der Kooy z tego samego uniwersytetu. - Oczywiście pierwszy wariant byłby lepszy. Pomóc oku wyleczyć się samemu? Rewelacja! Ale nawet jeśli nie wypali, to drugi jest na tyle obiecujący, że już teraz można mówić o wielkim, naprawdę wielkim sukcesie. Źródło: www.pbkm.pl, "Gazeta Wyborcza", "Science" |
Dzięki eksperymentalnej technice pierwszy raz udało się przywrócić możliwość widzenia ludziom cierpiącym na wrodzoną ślepotę Gen do wymiany Wrodzona ślepota Lebera to ciężka choroba siatkówki oka - zaburzenie rozwojowe czopków i pręcików wrażliwych na światło i odpowiadających za ostrość widzenia. Choroba ujawnia się we wczesnym dzieciństwie, stopniowo pozbawiając chorych możliwości widzenia. Na etapie wczesnej dorosłości zazwyczaj definitywnie tracą oni wzrok. Dotąd nie potrafiono jej leczyć. Dziś okazuje się, że możliwe jest naprawienie uszkodzeń w kodzie DNA i przywrócenie wzroku niewidzącym lub słabowidzącym. Aby tego dokonać, trzeba wadliwą wersję genu RPE65 wymienić na wersję nieuszkodzoną, która warunkuje powstanie białka o tej samej nazwie niezbędnego do przekazywania bodźców świetlnych przez fotoreceptory i przekazywania obrazów z siatkówki do mózgu. W tym celu naukowcy zaprosili do współpracy... wirus z grupy adenowirusów. Aby chciał współpracować, trzeba go było najpierw pozbawić tendencji do niszczenia komórek siatkówki. Unieszkodliwiony drobną modyfikacją genetyczną przestał stanowić zagrożenie dla człowieka. Można więc było przejść do następnego etapu działań, a więc zaprzęgnięcia wirusa do roli nośnika prawidłowej wersji uszkodzonego genu, którą naukowcy uzyskali z ludzkiego DNA. Jak wirus z człowiekiem współpracował Dlaczego jednak wirus miałby chcieć cokolwiek przenosić? Wirusy mają nadzwyczajną zdolność integrowania się z genomami swoich ofiar. Tym sposobem, przenikając do naszych komórek, mogą podmienić nieprawidłową wersję RPE65 na wersję działającą, która naprawi zniszczenia w komórkach oka. - Siatkówka dobrze nadaje się do terapii genowej, bo przez długie lata nie ulega zniszczeniu - powiedział dr Robin Ali kierujący zespołem naukowców w University College London. Tak też się stało w przypadku czterech z sześciu młodych pacjentów, którym wstrzyknięto zmodyfikowane adenowirusy do siatkówki. Terapia podziałała na wszystkie trzy osoby leczone w Pensylwanii i na jedną z trzech leczonych w Wielkiej Brytanii. Badania nad możliwościami terapii genowej prowadzone są już od 30 lat. Najpierw analizowano jej wpływ na psy i małpy, a od 15 lat naukowcy próbowali wdrożyć tę technikę w leczeniu ludzi. Najnowszy sukces dobrze wróży możliwościom leczenia tego typu schorzeń. Efekt działania wadliwego genu można porównać do brakującej świecy zapłonowej w silniku samochodu. Cały silnik może być w jak najlepszym porządku, ale gdy brak w nim świecy, nie uda się go zapalić. W komórkach siatkówki ludzi cierpiących na wrodzoną ślepotę Lebera brakuje białka niezbędnego do przekazywania bodźców świetlnych i obrazów do mózgu. Sposób leczenia niedostępny dla Polaków Rozmowa z dr. hab. Maciejem R. Krawczyńskim. Katedra i Zakład Genetyki Medycznej Uniwersytetu Medycznego w Poznaniu: Rz: Jak częstą chorobą jest wrodzona ślepota Lebera? Maciej R. Krawczyński: To rzadkie schorzenie. Ocenia się, że występuje u jednego na 30 tys. dzieci. Choroba ta jest odpowiedzialna za co piąty przypadek wrodzonej ślepoty w krajach rozwiniętych. Kto może na nią zapaść? To schorzenie dziedziczne. Jeśli wystąpiło u jednego dziecka, istnieje 25 proc. szans, że ujawni się również u jego rodzeństwa. Jakie są objawy choroby? Przede wszystkim pogorszenie ostrości wzroku, do ślepoty włącznie. U małych dzieci do trzeciego miesiąca życia mogą się pojawić oczopląs, światłowstręt, zanik aktywności fotoreceptorów i brak reakcji źrenicznych. Początkowo nie widać zmian zwyrodnieniowych na dnie oka, a dopiero około trzeciego roku życia pojawiają się tam plamki barwnika zwane skórą lamparta. Dzieci dotknięte tą chorobą często uciskają palcami oczy, drażniąc gałki oczne. Dlaczego to akurat schorzenie poddaje się terapii genowej? Badania nad terapią genową wrodzonej ślepoty Lebera zaszły tak daleko, ponieważ naukowcy od dawna dysponowali modelem zwierzęcym tego schorzenia. Po pierwszych sukcesach terapii u małp i psów przyszła kolej na ludzi. Sprawę ułatwia to, że zmiany chorobowe skupiają się na komórkach nabłonka barwnikowego siatkówki, a wirusy z grupy adenowirusów, dzięki którym wprowadzany jest prawidłowy gen, atakują właśnie komórki nabłonkowe. Czy można leczyć tę chorobę w inny sposób? Nie ma możliwości leczenia, można tylko ograniczyć jej skutki, stosując kurację witaminową i prowadząc rehabilitację wzrokową. To jednak nie daje zadowalających efektów. W zasadzie okuliści są wobec tej choroby bezradni. Kiedy możliwe będzie wprowadzenie terapii genowej w Polsce? Gdyby się znalazły fundusze, wprowadzenie tego w czyn byłoby wykonalne. Ogromne koszty czynią jednak terapię genową niedostępną dla Polaków. Więcej o nowej metodzie ratowania wzroku: www.ucl.ac.uk (źródło: Rzeczpospolita |
Szansa dla milionów osób zagrożonych schorzeniem AMD i retinopatią cukrzycową Autorem sukcesu jest zespół z University of Utah współpracujący z uczonymi z kilku innych ośrodków. Jak udało im się ustalić, uaktywnienie białka występującego w komórkach naczyń krwionośnych może nie tylko zapobiec chorobom oczu, ale także odwrócić zmiany. Co prawda badania w tym zakresie zostały przeprowadzone na myszach, ale ponieważ zakończyły się powodzeniem, naukowcy wierzą, że w przyszłości pomogą ludziom. - To odkrycie ma ogromne znaczenie dla opracowania środka, który będzie aktywizował Robo4, a w rezultacie leczył AMD i retinopatię - twierdzi prof. Kang Zhang, jeden z autorów badań. Jak działa to cudowne białko? Hamuje wzrost nieprawidłowych naczyń krwionośnych oraz powstawanie wycieków z nich, czyli powstrzymuje procesy, które leżą u podstaw AMD i retinopatii. Ale może być przydatne także w terapii innych chorób, których skutkiem jest uszkodzenie naczyń krwionośnych, np. SARS (zespół ostrej niewydolności oddechowej). Historycznymi nazwał ustalenia naukowców prof. Randall Olson, szef John A Moran Eye Center przy University of Utah. Bardzo pozytywnie zareagował na nie także prof. Roy Bicknell z University of Birmingham, który w latach 90. odkrył istnienie genu Robo4. - Jeśli za jego pomocą naprawdę można leczyć choroby oczu, jest to duże osiągnięcie - skomentował.Wyniki badań zostały opublikowane w piśmie "Nature Medicine". Źródło: "Rzeczpospolita" |
Szansa na przywrócenie wzroku Ludzkie oko to jeden z najbardziej skomplikowanych wynalazków natury. Tysiące wyspecjalizowanych komórek nerwowych umieszczonych na siatkówce potrafi zamieniać bodźce świetlne na impulsy nerwowe, na podstawie których w mózgu powstaje obraz oglądanego przez nas przedmiotu. Na skutek różnego rodzaju chorób może dojść do degeneracji fotoreceptorów siatkówki. Chory zaczyna widzieć coraz gorzej, aż w końcu - nieodwracalnie - traci wzrok. Takim osobom może pomóc wynalazek prof. Marka Humayuna z University of California. Elektroniczna proteza wzroku o nazwie Argus II składa się z trzech elementów: okularów z kamerą, wszczepianego do oka czipa oraz kieszonkowego urządzenia przetwarzającego informacje z kamery na odpowiedni sygnał przesyłany do czipa. Zabieg wszczepienia implantu ma trwać zaledwie godzinę. Jak działa Argus? Niezwykle prosto. Kamera wysyła sygnały o rejestrowanym przez nią obrazie do przenośnej, bezprzewodowej przystawki noszonej w kieszeni. Zadaniem przystawki jest zamiana sygnału wizualnego na sygnał pobudzający elektrody czipa z odpowiednią częstotliwością. „Sygnał trafia wpierw do odbiornika umieszczonego na gałce ocznej, a stamtąd do elektrod pobudzających nerw wzrokowy, podobnie jak czyniłyby to fotoreceptory” - wyjaśnia prof. Humayun. Cały proces odbywa się niezwykle szybko, zaledwie ulamki sekundy. Implant siatkówkowy to kilkumilimetrowa płytka z 60 niezależnymi mikroelektrodami, które potrafią generować prąd i pobudzać nerw wzrokowy. Co zobaczy osoba z nowym implantem? Zapewne znacznie więcej niż ludzie, którym wszczepiono Argusa I z wyposażonego w 16 elektrod. „Choć poprzedni implant był dość słaby wyniki eksperymentu przeszły nasze najśmielsze oczekiwania” - zauważa amerykański uczony. Spodziewano się, że chorzy odzyskają jedynie zdolność odróżniania ciemności i jasności. Okazało się jednak, że po kilku tygodniach „nauki” odczytywania nowych wrażeń ochotnicy potrafili odróżnić kubek od widelca, dostrzec okno, drzwi czy poruszające się obiekty. Mózg pacjentów dopowiadał brakujące informacje, dzięki czemu mogli wyciągać pełniejsze wnioski z tego, co widział sam czip. Jednym z pacjentów, którym wszczepiono pierwszą wersję implantu o małej rozdzielczości, był 58-letni Kalifornijczyk, Terry Byland. „Z początku widzenie z pomocą Argusa I przypominało patrzenie na kilka świecących punktów” - wspomina. „Teraz widzę znacznie więcej, np. kiedy przechadzam się po ulicy, potrafię dostrzec nisko zawieszone gałęzie. Dostrzegam też ludzkie twarze, choć są to dla mnie po prostu ciemniejsze plamy na jaśniejszym tle” - mówi. Co ciekawe, niektórzy pacjenci z wszczepionym implantem nie tylko widzą jasne punkty, ale też kolory. Zdaniem prof. Humayuna wrażenia barw biorą się z przypadkowego dobrania częstotliwości impulsów elektrycznych generowanych przez Argusa. „Może się zdarzyć, że implant podbudza nerw w tym samym rytmie, co zdrowe receptory reagujące na jakiś kolor” - wyjaśnia badacz. „Jeśli uda nam się rozszyfrować ?elektryczny? kod poszczególnych kolorów, być może, w kolejnej generacji implantów będziemy potrafili je odtwarzać, tak by chorzy widzieli barwny obraz” - mówi prof. Humayun. Nim to jednak nastąpi badacze planują testy nowej wersji implantów. Zostaną one przeprowadzone w pięciu ośrodkach badawczych i łącznie weźmie w nich udział ok. 75 osób. Zdaniem Humaya, czip o mocy 60 pikseli (każda elektroda to jeden świetlny punkt, który dostrzeże siatkówka) umożliwi pacjentom szybsze rozróżnianie obiektów. Urządzenie ma kosztować ok. 30 tys. dolarów, a więc podobnie co implant ślimakowy, który wszczepia się obecnie osobom niesłyszącym. Na tym jednak nie koniec badań prof. Humayuna. „Budowa pierwszego urządzenia zajęła nam 15 lat, a Argusa II zaledwie cztery. Biorąc pod uwagę postęp technologii, jestem przekonany, że już za 5 lat będziemy mogli zaproponować chorym implanty o rozdzielczości rzędu tysięcy pikseli, które umożliwią im rozpoznawanie twarzy” - opowiada uczony. Źródło: Dziennik |
Po raz pierwszy w historii udało się przeszczepić odbierające światło fotoreceptory. Dzięki nowatorskiej metodzie ślepe myszy odzyskały wzrok Niewidome myszy zareagowały na światło Fotoreceptory są częścią skomplikowanego systemu, który dostarcza sygnały wzrokowe do mózgu. Wyłapują światło i przekształcają je w chemiczne impulsy, które podróżując nerwem wzrokowym, trafiają do odpowiedniego ośrodka. Tam tworzy się widziany przez nas obraz. Naukowcy od dawna uważali, że choroby siatkówki związane z utratą fotoreceptorów można zwalczać terapią wykorzystującą komórki macierzyste. Dlaczego? Otóż nawet jeżeli w czasie choroby pręciki czy czopki zostaną zniszczone, to reszta drogi wzrokowej biegnącej do mózgu pozostaje nienaruszona. W ostatnich latach wielokrotnie próbowano więc przeszczepiać do chorych oczu komórki macierzyste pobrane z samej siatkówki lub różnych części centralnego systemu nerwowego. Niestety, wszystkie te próby zawiodły. Przeszczepiane komórki były co prawda w stanie przeżyć, ale nie potrafiły połączyć się z siatkówką ani tym bardziej przekształcić się w porządne fotoreceptory. - Doszliśmy do wniosku, że skoro „klasyczne” komórki macierzyste nie działają, to może należałoby spróbować z komórkami będącymi na trochę późniejszym etapie rozwoju - opowiada prof. Robin Ali z Instytutu Okulistycznego w Londynie, jeden z autorów badań. Do sprawdzenia swojej teorii naukowcy wykorzystali trzy grupy niewidomych, genetycznie zmodyfikowanych myszy. Cierpiały one na analogiczne jak u ludzi wrodzone choroby związane ze zwyrodnieniem siatkówki i utratą fotoreceptorów. Zwierzętom wszczepiano prekursory pręcików pobrane od zdrowych myszy będących na różnym etapie rozwoju - pod koniec ciąży i w pierwszym okresie po przyjściu na świat. Najlepsze rezultaty osiągnięto z komórkami pobranymi pomiędzy trzecim a piątym dniem po narodzinach. Pre-pręciki (dzięki inżynierii genetycznej świeciły na zielono, co pozwalało badaczom dokładnie je śledzić) z powodzeniem wędrowały do chorej siatkówki i tworzyły połączenia z obecnymi w niej wypustkami włókien nerwowych. Całkowicie niewidome myszy wkrótce po przeszczepie zaczynały reagować na światło. Klucz do znalezienia nowych terapii Oczywiście pozostaje pytanie - kiedy nową metodę będzie można zastosować u ludzi? - Na pewno musi minąć co najmniej kilka lat - uważa prof. Anand Swaroop z Uniwersytetu Michigan w USA, drugi z autorów badania (trzeci to dr Robert MacLaren ze Szpitala Okulistycznego w Londynie). Naukowcy będą musieli zmierzyć się z kilkoma trudnymi problemami. Przede wszystkim trzeci-piąty dzień po porodzie u myszy odpowiada mniej więcej drugiemu trymestrowi ciąży u ludzi. Jest oczywiste, że nikt nie poważy się w tym czasie na próbę pobrania komórek. Dlatego naukowcy będą musieli nauczyć się pozyskiwać pre-pręciki w inny sposób. Już teraz prowadzone są próby nad komórkami macierzystymi pobieranymi z siatkówki dorosłych osób (docelowo planuje się, że będzie to siatkówka samych pacjentów), które następnie dojrzewają do odpowiedniego momentu w warunkach laboratoryjnych. Poza tym człowiek będzie potrzebował do przeszczepu znacznie więcej komórek niż mysz - w naszym oku znajduje się ponad sto milionów fotoreceptorów. Na szczęście większość chorób degeneracyjnych atakuje centralną część siatkówki i tylko tam trzeba będzie wymienić zniszczone fotoreceptory. Naukowcy chcą też powtórzyć swoje doświadczenie, przeszczepiając tym razem wrażliwe na kolor czopki. Mimo wszystkich tych problemów okrycie opisane w listopadowym „Nature” (2006) jest niewątpliwym przełomem. Naprawienie komórek tworzących szlaki nerwowe w ludzkim mózgu od lat jest jednym z największych wyzwań medycyny. Zdaniem ekspertów to klucz do znalezienia nowych terapii nie tylko dla oczu, ale też do walki z takimi chorobami układu nerwowego, jak Alzheimer, Parkinson albo nieuleczalne dziś urazy rdzenia kręgowego. (źródło: Gazeta Wyborcza, Nature) |
„Nowiny z dziedziny nauki”
| Do Strony Głównej | Powrót | ||||
© Copyright by RETINA FORUM 2001-2016
redaktor naczelny: Piotr Stanisław Król
RETINA FORUM - Internetowe ok(n)o wiedzy genetycznej


